Bakteriocine
Neue Antibiotika-Alternativen aus Bodenbakterien
Bakterien sind nicht allzu freundlich untereinander: viele von ihnen geben antimikrobielle Stoffe in ihre Umgebung ab, um sich so in ihrer ökologischen Nische Vorteile zu verschaffen. Solche Bakteriocine machen sich Forschende der Universität Ulm zunutze: Sie haben ein gentechnisch verändertes Bodenbakterium geschaffen, das als biotechnologischer Plattformorganismus solche Antibiotika-Alternativen rein und in großer Menge produzieren kann – und das auch noch ressourcenschonend aus Abfallstoffen.
Lassen Mensch und Tier gerne mal die Muskeln spielen, um unliebsame Konkurrenz aus dem Revier zu vertreiben, so haben Mikroorganismen nichts Derartiges zur Hand. Dafür etwas umso Drastischeres: Bakteriocine. Diese kleinen, antimikrobiellen Peptide werden von einer Vielzahl von Bakterien produziert und sind in der Lage, die Zielorganismen abzutöten oder zumindest ihr Wachstum zu hemmen. Ihre biologische Rolle besteht darin, dem Produzenten Überleben und Ausbreitung in seiner ökologischen Nische zu sichern.
Aber auch für uns sind Bakteriocine von Bedeutung: Aufgrund der Aktivität gegen Krankheitserreger werden sie schon vielfach als Konservierungsstoffe in Lebensmitteln und Tierfutter eingesetzt. Nisin beispielsweise, das hinter der Nummer E 234 steckt: Diese antimikrobielle Substanz dient dem Milchsäurebakterium Lactococcus lactis zur Porenbildung in fremden Biomembranen – ein für den Konkurrenzorganismus toxischer Vorgang. Für Menschen und Tiere sind Bakteriocine allerdings völlig harmlos. Sie gehören, wie beispielsweise in der Milch, zu den natürlichen Nahrungsbestandteilen und werden im Verdauungstrakt schnell abgebaut.
Mit Bakteriocinen Antibiotika-Resistenzen vermeiden
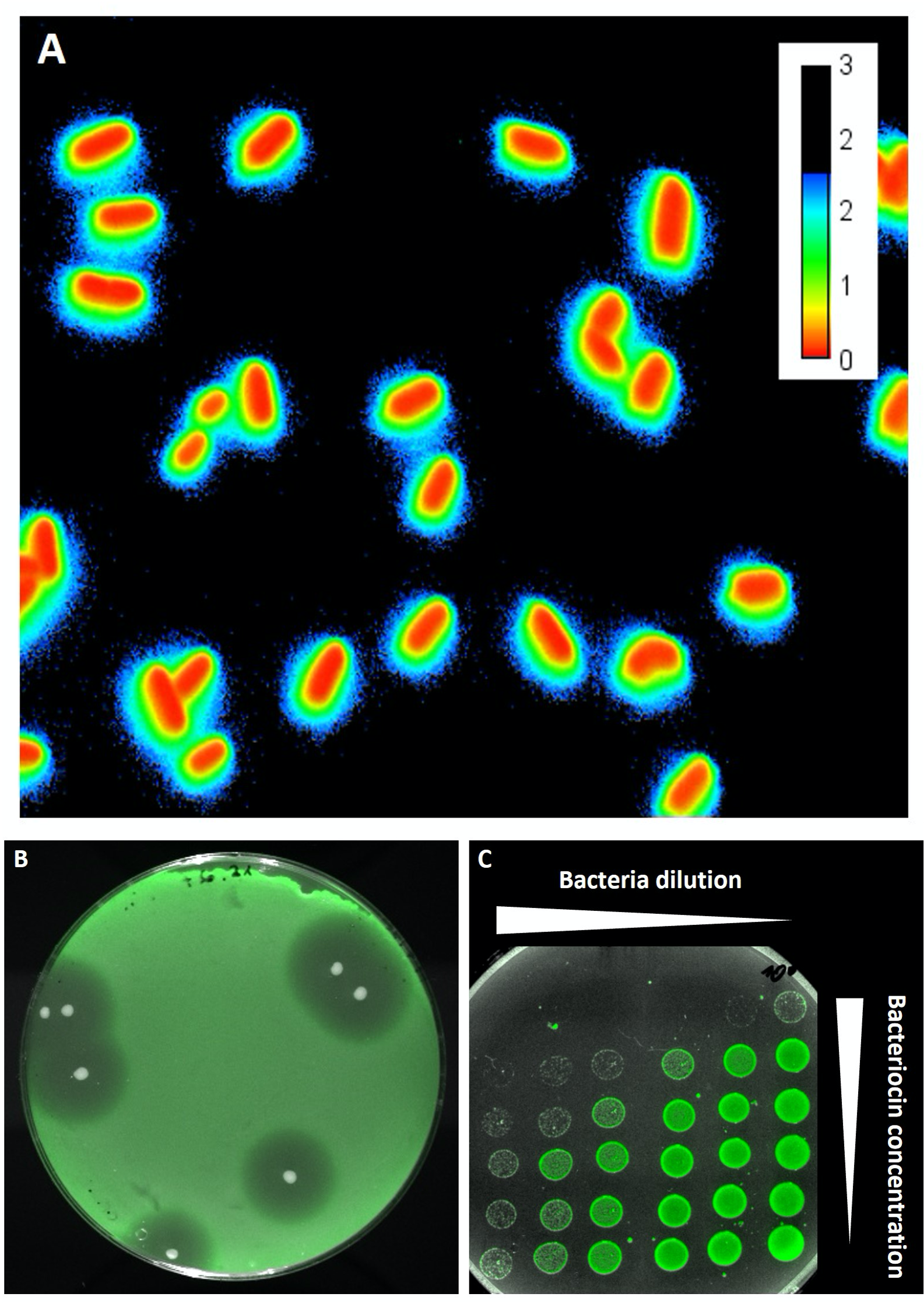 Die fluoreszenzmikroskopischen Aufnahmen zeigen in A) einzelne Bakterien und in B) sowie C) Kulturen auf Agarplatten. A) Mithilfe von fluoreszierenden Sensorbakterien könnten Bakteriocine detektiert werden: Sie leuchten im Außenbereich blaugrün, sobald sie in Kontakt mit der antimikrobiellen Substanz kommen. B) Rund um die weißen Kolonien der Bakteriocinproduzenten sind Hemmhöfe im Rasen der Sensorbakterien zu erkennen. C) Das Wachstum der Sensorbakterien wird gehemmt – wie stark, ist abhängig von Verdünnung sowie Bakteriocinkonzentration. © Christian Riedel / Universität Ulm
Die fluoreszenzmikroskopischen Aufnahmen zeigen in A) einzelne Bakterien und in B) sowie C) Kulturen auf Agarplatten. A) Mithilfe von fluoreszierenden Sensorbakterien könnten Bakteriocine detektiert werden: Sie leuchten im Außenbereich blaugrün, sobald sie in Kontakt mit der antimikrobiellen Substanz kommen. B) Rund um die weißen Kolonien der Bakteriocinproduzenten sind Hemmhöfe im Rasen der Sensorbakterien zu erkennen. C) Das Wachstum der Sensorbakterien wird gehemmt – wie stark, ist abhängig von Verdünnung sowie Bakteriocinkonzentration. © Christian Riedel / Universität UlmAuch medizinisches Potenzial wird in den Bakteriocinen schon seit einiger Zeit gesehen: Sie gelten als hoffnungsvolle Alternativen zu gängigen Antibiotika. Dadurch, dass Antibiotika in den letzten Jahren übermäßig und vor allem in der Tierhaltung geradezu missbräuchlich eingesetzt wurden, sind viele Krankheitserreger mittlerweile resistent gegen die einst sehr wirksame medizinische Waffe geworden. Bakterielle Resistenzen gehören laut Weltgesundheitsorganisation WHO zu den derzeit größten Bedrohungen unserer Gesundheit.1)
Tatsächlich wurden in den letzten Jahren auch schon eine Reihe von Bakteriocinen aus unterschiedlichsten Quellen gewonnen, die vielversprechende Wirkungen gegen klinisch relevante Krankheitserreger zeigen. Allerdings wurde deren praktische Anwendung bislang durch mehrere Faktoren verhindert: Sie müssen in aufwendigen Fermentationsprozessen mit natürlichen Bakterien hergestellt werden, für die es komplexe und teure Nährmedien braucht. Bestenfalls entstehen hieraus dann halbgereinigte Präparate oder Rohfermente, die für einen medizinischen Einsatz noch sehr aufwendig gereinigt werden müssen. Zudem ist der Energiebedarf der gesamten Prozedur hoch – für andere Anwendungen als die Lebensmittelkonservierung also viel zu kompliziert und unrentabel.
Bis jetzt –, denn eine Lösung ist in greifbarer Nähe: Forschende am Institut für Mikrobiologie und Biotechnologie der Universität Ulm haben gezeigt, dass es biotechnologisch möglich ist, mithilfe des industriellen Plattformorganismus Corynebacterium glutamicum – einem nicht-pathogenen Bodenbakterium – ein hochwirksames antimikrobielles Peptid so herzustellen, dass dies auch in den großtechnischen Maßstab übertragbar ist.2) „Wir haben gemeinsam mit europäischen Partnern im Projekt iFermenter einen Produktionsprozess entwickelt, mit dem wir Bakteriocine rekombinant, effizient und ressourcenschonend großtechnisch herstellen können“, berichtet Prof. Dr. Christian Riedel, der die Forschungsarbeiten in Ulm leitet. „Zunächst Pediocin PA-1, ein Peptid, das besonders gut gegen Listerien wirkt, wie sie beispielsweise in Rohmilch vorkommen und gefährliche Krankheitssymptome auslösen können. Nun wollen wir das Verfahren Stück für Stück auch auf andere Peptidpharmazeutika ausweiten und das Produktportfolio erweitern – nicht nur Antibiotika-Alternativen herstellen, sondern beispielsweise auch Hormone oder antivirale Substanzen.
Bakteriocinproduktion als modulares System
 Die Forschenden Dr. Oliver Goldbeck, Prof. Dr. Christian Riedel, Dominique N. Desef und Prof. Dr. Bernhard J. Eikmanns (v. l.) haben ein rekombinantes Bodenbakterium geschaffen, das Bakteriocine effizient produzieren kann (Auf dem Foto fehlt Dominik Weixler). © Lisanne Wolters / Universität Ulm
Die Forschenden Dr. Oliver Goldbeck, Prof. Dr. Christian Riedel, Dominique N. Desef und Prof. Dr. Bernhard J. Eikmanns (v. l.) haben ein rekombinantes Bodenbakterium geschaffen, das Bakteriocine effizient produzieren kann (Auf dem Foto fehlt Dominik Weixler). © Lisanne Wolters / Universität UlmUm Pediocin PA-1 herzustellen, haben die Forschenden die Corynebakterien gentechnisch verändert: Hierzu wurde das Gen eingebracht, das für die Bakteriocin-Biosynthese verantwortlich ist plus die erforderlichen Gene für Modifikations- und Transportproteine – aber nicht nur das. Weitere künstliche Gene verleihen den Bakterien die Fähigkeit, Abfallströme als Substrat zu nutzen. „Solche Abfälle, z. B. Lignocellulose-Hydrolysate aus der Holzindustrie, enthalten viele interessante Zucker“, erklärt Riedel. „Diese Zucker können dann von „unseren“ Bakterien zur Herstellung höherwertiger Produkte wie z. B. Bakteriocine genutzt werden.“
Überhaupt soll das System letzten Endes einmal modular aufgebaut sein: Die genetische Umgebung für das Grundsätzliche bleibt, und man würde dann nur noch Gene als Module für Substrat und Produkt nach Belieben austauschen. So könnte man je nach Bedarf unterschiedliche Substanzen herstellen, aber auch verschiedene Abfälle nutzen.
Weitere Produkte sind in Arbeit
Was das Pediocin PA-1 angeht, so ist das internationale Team derzeit dabei, das Verfahren vom Labor- in den großtechnischen Maßstab für die zukünftige Industrieproduktion zu überführen: „Gemeinsam mit unseren belgischen Partnern testen wir dies gerade in einem vorindustriellen 150-Liter-Maßstab“, berichtet der Professor. „Parallel erarbeiten wir uns weitere, auch komplexere Produkte, wie beispielsweise Nisin.“
Eine Herausforderung ist die Tatsache, dass die Bodenbakterien dank ihrer künstlichen Gene einerseits Substanzen produzieren sollen, die antimikrobiell wirken. Diese aber anderseits dem Produzenten selbst nicht schaden sollen. Im Falle von Pediocin kein Problem: Corynebacterium glutamicum besitzt keine Rezeptoren für das Bakteriocin. Für andere Substanzen, wie z. B. Nisin, könnte das aber durchaus schwierig werden. Deshalb bedienen sich die Experten eines Tricks: Zunächst einmal wird eine inaktive Vorstufe gebildet, die dann erst in einem zweiten Schritt aktiviert wird.
Tests in Cremes und Verbandsmaterial stehen bevor
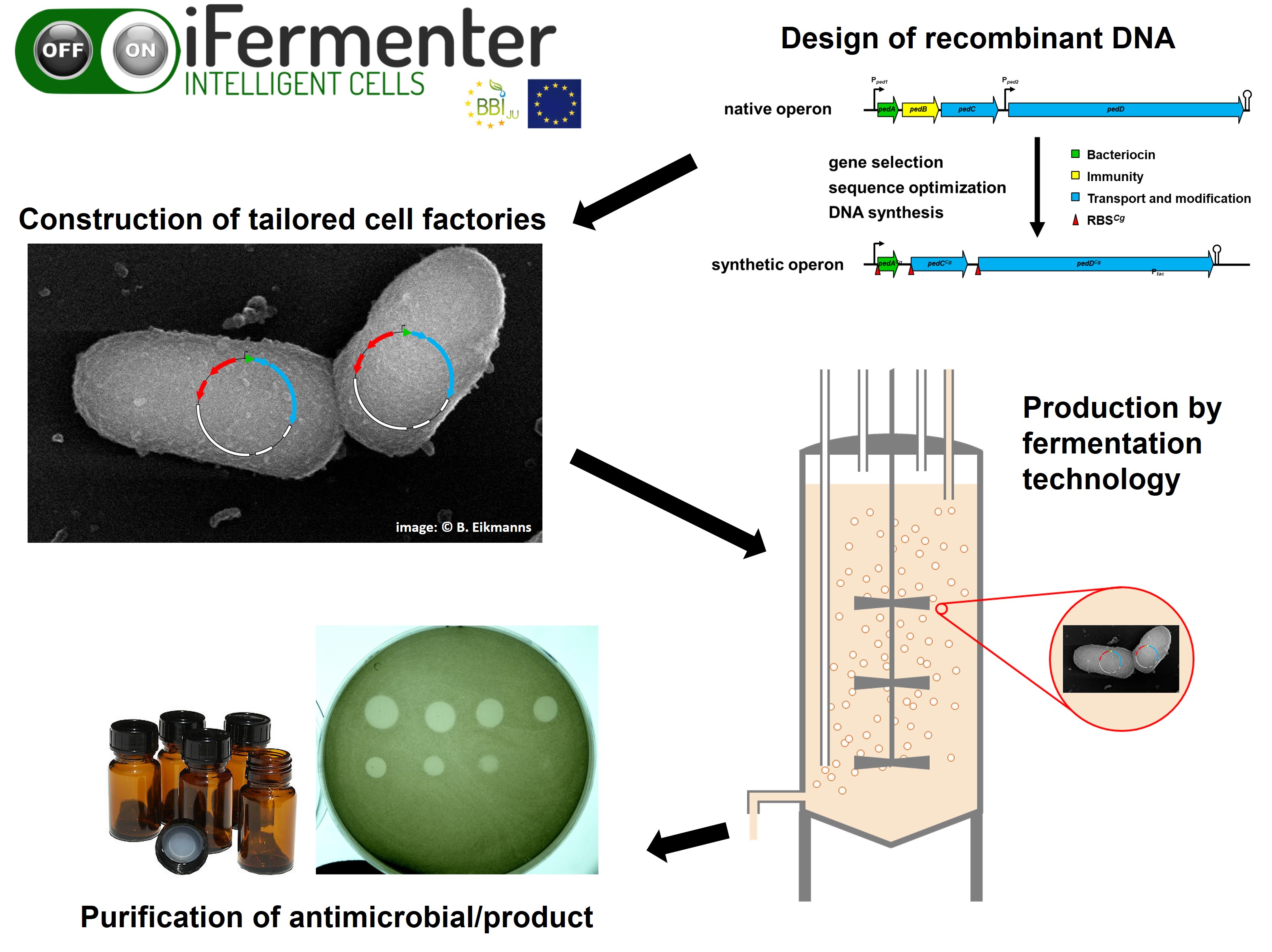 Im Forschungsprojekt iFermenter wurde mithilfe des Modellorganismus Corynebacterium glutamicum die rekombinante Produktion von Bakteriozinen etabliert, um sie zur medizinischen Nutzung zur Verfügung zu stellen. © Christian Riedel / Universität Ulm
Im Forschungsprojekt iFermenter wurde mithilfe des Modellorganismus Corynebacterium glutamicum die rekombinante Produktion von Bakteriozinen etabliert, um sie zur medizinischen Nutzung zur Verfügung zu stellen. © Christian Riedel / Universität UlmDen ersten Praxistest sollen die Bakteriocine in antimikrobiellen Cremes und Verbandsmaterial bestehen. „Ein Antrag gemeinsam mit dem Medizinproduktehersteller Hartmann läuft“, sagt Riedel. Denn für eine orale Anwendung eignen sich die Substanzen nicht. Sie würden im Magen-Darm-Trakt unschädlich gemacht, und auch intravenös verabreicht relativ schnell vom Immunsystem eliminiert werden. Deshalb konzentrieren sich die Forschungsaktivitäten auf die oberflächliche Anwendung, etwa auf Haut und Schleimhäuten. Aber auch als Probiotika in Kapseln zur Mikrobiom-Modifizierung wäre eine Nutzung denkbar. Viel zu tun haben die Ulmer Forschenden in nächster Zeit auf jeden Fall: Neben der Weiterentwicklung des schon Erreichten, wollen sie die Suche nach Antibiotika-Alternativen in alle möglichen Richtungen ausdehnen – Stammsammlungen durchmustern, Bodenproben analysieren oder in der Grundlagenforschung nach neuen Substanzen fahnden. Und dann natürlich ihr entwickeltes Verfahren möglichst schnell kommerzialisieren.
Projekt iFermenter
Die Ulmer Forschungsarbeiten rund um die Bakteriocine sind Teil des internationalen Forschungsverbundes iFermenter, der von der EU im Rahmen von Horizon 2020 mit rund 5,25 Mio. Euro gefördert und von der Norwegian University of Science and Technology koordiniert wird. Das Verbundvorhaben entwickelt intelligente Bioprozesstechnologien, um antimikrobielle Peptide aus Abfällen der Holzindustrie herzustellen. Der Forschungsverbund hat die Ziele, nicht nur zuckerhaltige Reststoffströme einer Wertschöpfung zuzuführen, sondern auch gleichzeitig deren Produktionsprozesse günstiger und ressourcenschonender zu gestalten.