Photoimmuntherapie
Lichtschalter gegen den Tumor: Wie man mit Photonen den Prostatakrebs in die Knie zwingen kann
Prostatakrebs ist die häufigste Krebserkrankung bei Männern in Deutschland. Trotz moderner Operationsmethoden wie der Da-Vinci-Roboter-Chirurgie bleiben Rückfälle und belastende Nebenwirkungen herkömmlicher Therapien eine Herausforderung. In der Klinik für Urologie des Uniklinikums Freiburg arbeitet Dr. Isis Wolf an der Weiterentwicklung der Photoimmuntherapie, einem vielversprechenden Ansatz, der künftig einen molekularen Meilenstein in der Krebsforschung darstellen könnte. Diese Methode nutzt Licht, Antikörper und einen speziellen Farbstoff, um Tumorzellen mit chirurgischer Präzision auszuschalten und gleichzeitig das Immunsystem zu „wecken“.
Die Crux beim Prostatakarzinom ist, dass es im Frühstadium kaum Symptome verursacht, während die Heilungschancen noch sehr hoch sind. Wenn Beschwerden beim Wasserlassen oder Knochenschmerzen auftreten, hat der Tumor oft schon gestreut. Die übliche Therapie der vollständigen Entfernung der Prostata, der radikalen Prostatektomie, führt in bis zu 40 Prozent der Fälle zu einem Rezidiv. Zudem drohen Nebenwirkungen wie Inkontinenz oder Impotenz, da im OP-Bereich sensible Nervenbahnen verlaufen. Dr. Isis Wolf arbeitet mit der Arbeitsgruppe Antikörper-basierte Diagnostik und Therapie am Uniklinikum Freiburg an einer schonenden molekularbiologischen Ergänzung zur Operation, die die Rezidivrate senken soll.
Ein molekulares Navigationssystem
 Die Biologin Dr. Isis Wolf widmet sich an der Uniklinik Freiburg dem Prostatakrebs und möchte mithilfe der Photoimmuntherapie die Heilungschance erhöhen und die Rezidivrate senken. © Fionn Große, privat
Die Biologin Dr. Isis Wolf widmet sich an der Uniklinik Freiburg dem Prostatakrebs und möchte mithilfe der Photoimmuntherapie die Heilungschance erhöhen und die Rezidivrate senken. © Fionn Große, privatDie Idee ist clever: Ein Medikament sucht selbstständig den Tumor, dockt an und wartet auf ein Signal, um die Zelle von innen heraus zu sprengen. Das Herzstück der Photoimmuntherapie (PIT) ist die Kombination aus biologischer Zielgenauigkeit und physikalischer Energie in Form von Licht.
Genau hier knüpft Wolf mit ihrer Forschung an. Damit die Therapie nur die Krebszellen trifft, nutzt sie ein spezielles Protein als Ankerpunkt: das Prostata-spezifische Membranantigen (PSMA). Dieses Protein findet sich in extrem hoher Dichte auf der Oberfläche von Prostatakrebszellen, während gesundes Gewebe es kaum produziert.
Auch kann PSMA als Marker fungieren, um den Fortschritt der Erkrankung zu definieren. In Wolfs Arbeitsgruppe werden künstlich hergestellte Antikörper eingesetzt, die wie ein Schlüssel zum Schloss exakt an dieses PSMA binden. „Wir haben einen sogenannten Photosensitizer entwickelt, einen speziellen Fluoreszenzfarbstoff aus der Gruppe der Phthalocyanine, der durch Licht aktiviert werden kann“, erklärt Wolf das Verfahren. „Diesen koppeln wir an die Antikörper und erhalten ein Antikörper-Wirkstoff-Konjugat, das wir auf die Krebszellen geben.“ So ist gewährleistet, dass nur Tumorgewebe adressiert wird. Gleichzeitig macht der Farbstoff die Zielzellen sichtbar: Bei schwacher Anregung erscheint er unter dem Mikroskop als rotes Fluoreszenzsignal.
Gezielter Zelltod durch Photonen
Solange kein Licht auf das Konjugat fällt, bleibt es völlig inaktiv. Erst bei Bestrahlung mit harmlosem Rotlicht einer Wellenlänge von 692 nm aktiviert das Licht den Fluoreszenzfarbstoff, und es kommt zur Zerstörung der Zelle. Molekularbiologisch löst das Licht eine Kettenreaktion aus: Der aktivierte Farbstoff schädigt die Krebszelle so massiv, dass ihre Zellmembran Poren bildet. „Durch diese Poren können Ionen und Wasser einströmen und nach etwa fünf Stunden platzen die Zellen dann“, sagt die Biologin. „Diesen Zelltod nennt man Pyroptose.“ Der Vorgang ist nicht nur deshalb hocheffizient, weil er extrem lokal wirkt und umliegendes Gewebe schont, sondern auch, weil der Tumor gleichzeitig durch den fluoreszierenden Farbstoff sichtbar gemacht wird. Dies könnte zukünftig helfen, den Tumor noch präziser zu entfernen.
Wolfs Wunsch wäre es, diese Therapie einmal OP-begleitend zur radikalen Prostatektomie anbieten zu können und damit die Rezidivrate zu senken. Ihre Idee: Dem Patienten am Tag vor der OP das Konjugat intravenös zu verabreichen und kurz nach der Entnahme der Prostata - während diese in der Pathologie untersucht wird und der Patient noch im OP ist - den OP-Roboter mit einer Laserfaser an die entsprechende Stelle zu führen, um dort zu beleuchten. „Man könnte das quasi als Add-on machen, um die restlichen Tumorzellen noch zu erreichen“, sagt die Trägerin des Klaus-Mangold-Preises. Nebenwirkungen wären hier minimal, da die Aktivierung durch das Licht nur auf den OP-Bereich begrenzt bleibt.
Weckruf für das Immunsystem
Was die PIT jedoch zu einem echten Hoffnungsträger macht, ist der sogenannte immunogene Zelltod. Wenn die Krebszellen durch den Lichtimpuls zerstört werden, setzen sie Bruchstücke ihres Inneren und Warnsignale frei. Das Immunsystem, das den Krebs zuvor ignoriert hat, erkennt diese Signale plötzlich als Gefahr, und Abwehrzellen werden scharfgeschaltet. Es ist, als würde man dem Körper eine „Impfung“ von innen verabreichen.
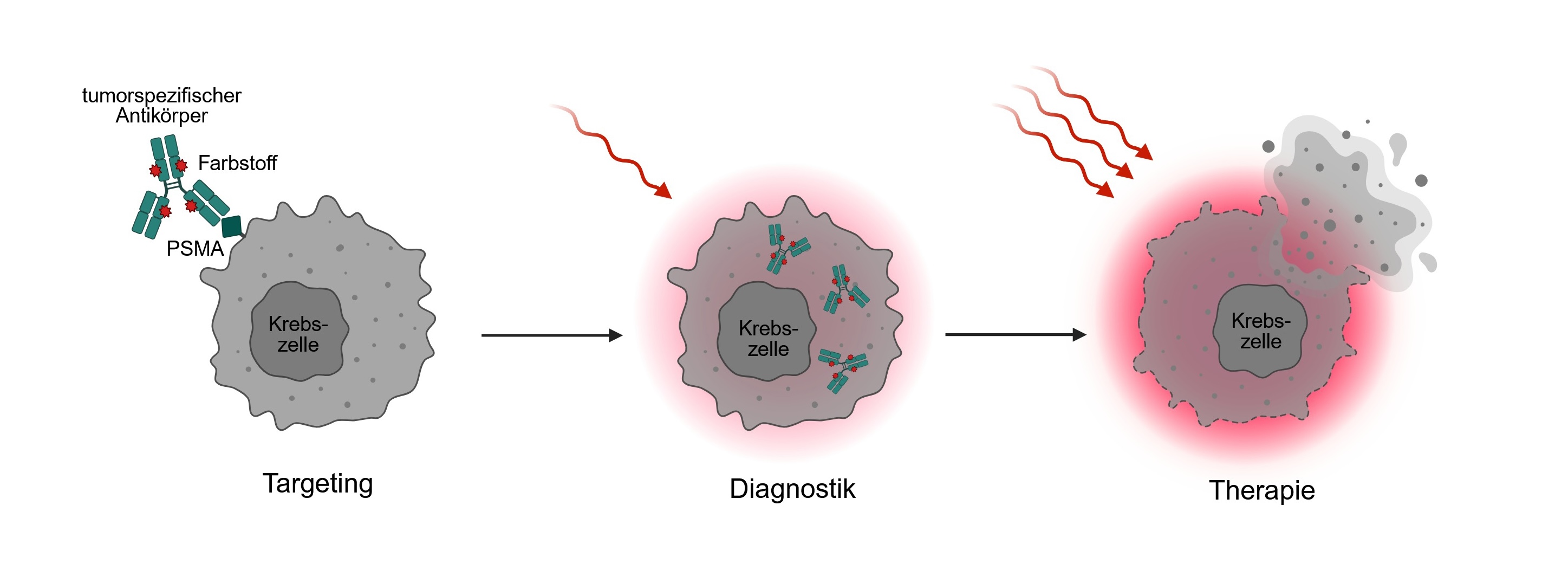 Nachdem das Konjugat aus tumorspezifischem Antikörper und Farbstoff an der PSMA-Struktur der Tumorzelle andockt, wird es in die Zelle aufgenommen. Bei Bestrahlung mit Infrarotlicht wird der Zelltod (Pyroptose) ausgelöst: Die Zelle platzt. © Created in BioRender. Wolf, I. T. (2026) https://BioRender.com/f1kvu6b
Nachdem das Konjugat aus tumorspezifischem Antikörper und Farbstoff an der PSMA-Struktur der Tumorzelle andockt, wird es in die Zelle aufgenommen. Bei Bestrahlung mit Infrarotlicht wird der Zelltod (Pyroptose) ausgelöst: Die Zelle platzt. © Created in BioRender. Wolf, I. T. (2026) https://BioRender.com/f1kvu6b
Wolf würde in Zukunft gern bei dieser Aktivierung des Immunsystem mittels immunkompetenter Mäuse herausfinden, ob die Therapie auch systemisch wirkt. „Meine Hoffnung wäre, auch die versteckten Metastasen anzuvisieren, die man mit der OP nicht hat erwischen können“, erläutert sie. Eine denkbare Nebenwirkung der Immunstimulation wäre jedoch, dass man überstimuliert und einen Zytokin-Sturm auslöst, so wie es bei der CAR-T-Zell-Therapie auch der Fall sein kann. Da aber mit der PIT nur residuale (restliche) Tumorzellen angesprochen werden sollen, schätzt Wolf dieses Risiko als gering ein.
Ferner möchte die Forscherin in einem Folgeprojekt noch untersuchen, wo genau sich das Konjugat innerhalb der Zelle nach der Aufnahme befindet und was genau damit passiert.
Ausblick über die Prostata hinaus
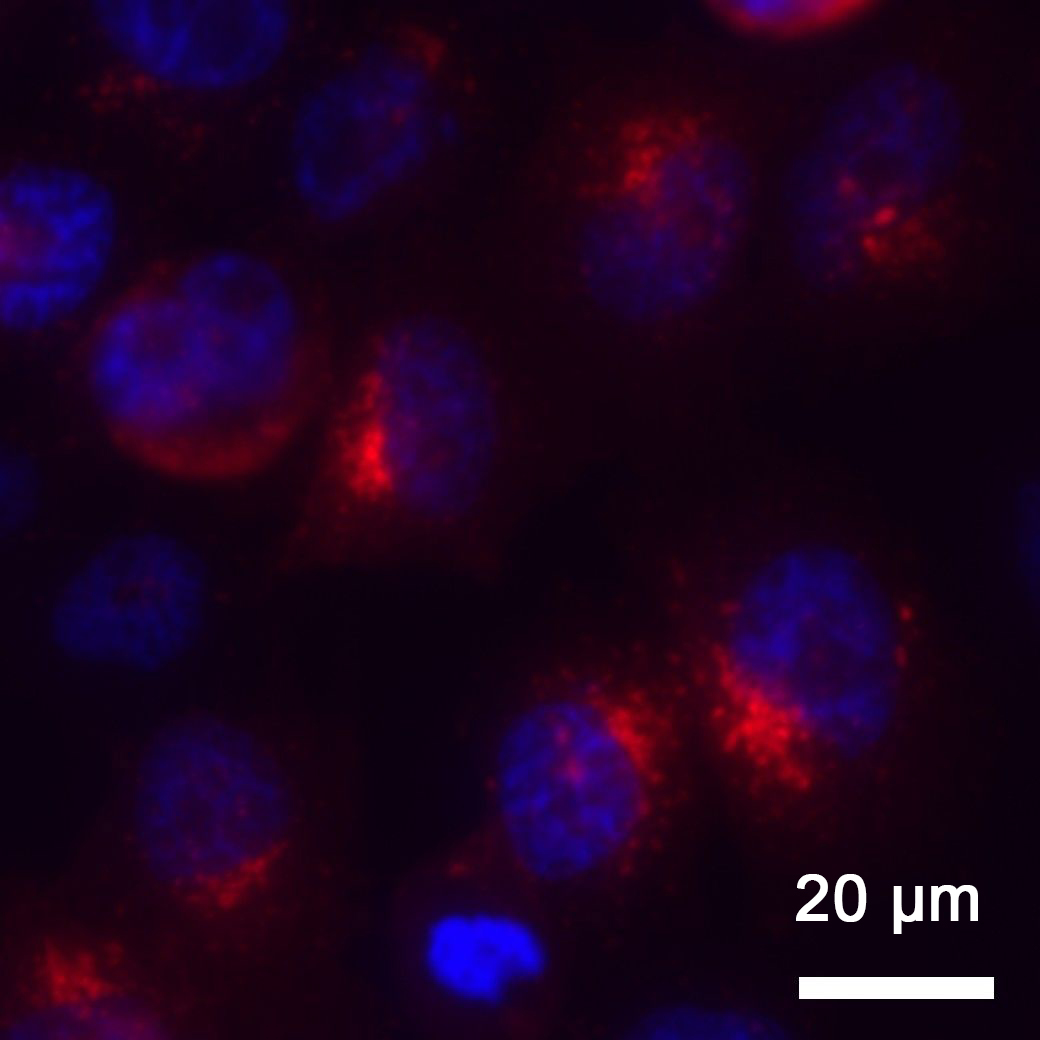 Unter dem Mikroskop werden die Tumorzellen des Prostatakarzinoms mit ihren blauen Zellkernen sichtbar. Die roten Fluoreszenz-Signale zeigen innerhalb der Zellen die Anreicherung des Konjugats aus Antikörper und Farbstoff nach Bindung an PSMA-Strukturen an. © Dr. Isis Wolf, Uniklinik Freiburg
Unter dem Mikroskop werden die Tumorzellen des Prostatakarzinoms mit ihren blauen Zellkernen sichtbar. Die roten Fluoreszenz-Signale zeigen innerhalb der Zellen die Anreicherung des Konjugats aus Antikörper und Farbstoff nach Bindung an PSMA-Strukturen an. © Dr. Isis Wolf, Uniklinik FreiburgTrotz der positiven Ergebnisse in der Präklinischen Phase ist der Weg in die tägliche Praxis noch weit. So müssen alle Faktoren wie Antikörper, Farbstoff sowie das Konjugat einzeln klinisch zugelassen werden. Wolf hofft, auf schon zugelassene Antikörper zurückgreifen zu können und so eine zeitliche Abkürzung zu nehmen. Dank eines Förderbeitrags der wissenschaftlichen Gesellschaft Freiburg testet sie das Verfahren bereits gegen Darmkrebs und hat auch schon Brust- und Blasenkrebs im Visier. Somit könnte aus der Photoimmuntherapie gegen Prostatakrebs ein modulares System werden, bei dem lediglich die Antikörper ausgetauscht werden müssten, um verschiedene Tumorentitäten zu adressieren.
Die Forscherin wurde für ihren vielversprechenden Ansatz im Dezember 2025 mit dem Klaus-Mangold-Preis ausgezeichnet. Der vom Uniklinikum Freiburg 2024 ins Leben gerufene Preis würdigt herausragende Projekte zur besseren Versorgung von Patientinnen und Patienten. Wolf sieht diesen Preis als Anerkennung und Ansporn, ihre Forschung nach außen zu tragen und weiterhin an einer Alternative zur Chemotherapie zu arbeiten, um die Krebstherapie von morgen präziser zu gestalten. Denn die Vision einer schonenderen Heilung treibt sie an, und so formuliert sie ihren Wunsch für die Zukunft: „Meine Hoffnung ist, dass unser Konstrukt eines Tages in der Klinik eingesetzt werden kann, Rezidive reduziert und Erkrankten eine schonendere Behandlung ermöglicht.“