Immunkomplexe bei COVID-19
Teufelskreis der Hyperinflammation
Ob man nach einer Coronainfektion nur ein leichtes Unwohlsein oder einen kritischen Verlauf erlebt, hängt offenbar von Antigen-Antikörper-Komplexen ab, die in unserem Körper gebildet werden. Die entdeckten Immunkomplexe führten die Forschenden um Prof. Dr. Hartmut Hengel von der Uniklinik Freiburg auf die Spur eines sich verstärkenden Teufelskreises der Entzündung. Das Immunsystem wird unkontrolliert angetrieben, was zu einem kritischen Fortschreiten der Erkrankung führt. Für potenzielle Therapien bietet diese Erkenntnis eine vielversprechende Grundlage.
Oft ist es nur ein kleiner Husten und Fieber, aber in einigen Fällen ist nach einer Ansteckung der ganze Körper betroffen und eine mechanische oder sogar extrakorporale Beatmung nötig. Es gibt zunehmend klinische und experimentelle Hinweise darauf, dass körpereigene Moleküle dafür verantwortlich sind. Der Virologe Prof. Dr. Hartmut Hengel vom Uniklinikum Freiburg fand mit seinem Team heraus, was die Infektion mit dem Coronavirus, die primär im Atemtrakt in Erscheinung tritt, so gefährlich macht und erklärt, warum Menschen plötzlich Multiorganversagen bekommen. Schwere Verläufe werden dabei nicht durch das Virus selbst, sondern durch die körpereigene Abwehr hervorgerufen. Das Immunsystem, das den Körper eigentlich schützen soll, reagiert so stark, dass der Segen einer starken Abwehr zum Fluch wird. „Die Immunantwort ist ein großes Konzert mit sehr vielen Instrumenten und verschiedenen Melodien“, sagt Hengel. „Die Antikörper sind neben T-Zellen, Botenstoffen und spezifischen Immunzellen nur ein Teil davon.“
Immunkomplexe als Akteure identifiziert
 Prof. Dr. Hartmut Hengel hat gemeinsam mit seinem Team den Mechanismus aufgeklärt, wie es bei COVID-19 zu schweren Verläufen kommen kann. © Prof. Dr. Hartmut Hengel, Uniklinik Freiburg
Prof. Dr. Hartmut Hengel hat gemeinsam mit seinem Team den Mechanismus aufgeklärt, wie es bei COVID-19 zu schweren Verläufen kommen kann. © Prof. Dr. Hartmut Hengel, Uniklinik FreiburgDie Forschenden um Hengel fahndeten nach den Verursachern der Immunüberreaktion und stießen auf große Komplexe aus Antigenen und Antikörpern, die fast ausnahmslos bei Patientinnen und Patienten mit schwerem COVID-Verlauf auftraten. Erstaunlicherweise befanden sich in diesen Immunkomplexen jedoch weder Virusmaterial noch virusspezifische Antikörper. „Wir denken, dass das mit dem Virus selbst gar nicht viel zu tun hat“, erklärt der Virologe. Nur körpereigene Moleküle (Selbst-Antigene) und gegen sie gerichtete Antikörper (Autoantikörper) scheinen Bestandteil dieser Aggregate zu sein. „Und diese Immunkompexe führen dann zur immunologischen Selbstvernichtung des Körpers.“ Ihr Auftreten wurde schon in der Vergangenheit oft mit einem schweren Krankheitsverlauf bei Autoimmunkrankheiten in Verbindung gebracht, etwa dem systemischen Lupus Erythematodes (SLE) oder der rheumatoiden Arthritis.
Die Tatsache, dass in kritischen Fällen plötzlich das Gehirn und die Niere angegriffen sind, in denen sich auch nicht viel Virusmaterial findet, bestärkte die Forschenden in ihrer Annahme. Im Gegensatz zu den im Gewebe festsitzenden Antigen-Antikörper-Komplexen sind besonders die löslichen und frei in der Blutbahn zirkulierenden Immunkomplexe dafür verantwortlich, dass die Entzündung im ganzen Körper verteilt wird. Ein frühzeitiger Nachweis der Komplexe nach klinischer Verschlechterung könnte ein Indikator für die Notwendigkeit einer sofortigen entzündungshemmenden Therapie sein.
Überreaktion durch Autoimmunität?
 Das Team um Prof. Dr. Hartmut Hengel: Dr. Philipp Kolb, Dr. Valeria Falcone, Dr. Sebastian Giese am Universitätsklinikum Freiburg (v. links nach rechts). © Prof. Dr. Hartmut Hengel, Uniklinik Freiburg
Das Team um Prof. Dr. Hartmut Hengel: Dr. Philipp Kolb, Dr. Valeria Falcone, Dr. Sebastian Giese am Universitätsklinikum Freiburg (v. links nach rechts). © Prof. Dr. Hartmut Hengel, Uniklinik FreiburgWenn man die Überreaktion des Immunsystems, die in eine Überentzündung (Hyperinflammation) mündet, auf die Bildung von gegen den eigenen Körper gerichteten Autoantikörpern zurückführen kann, ergibt sich das Phänomen der Autoimmunität. Die Forschenden vermuten, dass dies auch hier ein Teil des Mechanismus ist, aber noch nicht die ganze Wahrheit hinter den schweren COVID-Verläufen.
Es gibt zudem weitere Mechanismen der Überreaktion, wenn etwa aktivierende Rezeptoren auf Immunzellen exprimiert werden, die dort üblicherweise nicht anzutreffen sind. Auch kann eine veränderte Zuckermolekülsignatur auf Antikörpern, die gegen das Virus gerichtet sind, eine höhere Reaktivität der betroffenen Antikörper mit sich bringen, wenn diese von Immunzellen erkannt werden. Beides führt zur Hyperinflammation und ist in Erkrankten mit schweren Verläufen beschrieben worden: Die virusspezifischen Antikörper, die aufgrund der veränderten Zuckersignatur eine zu starke Effektorfunktion besitzen, binden an Rezeptoren, die auf den falschen Zellen sitzen. Hinzu kommen die löslichen Immunkomplexe, die ihrerseits zusätzlich die normale Immunantwort verstärken. „Wir glauben, dass das in einem Zusammenhang steht, und dass die eine Überreaktion die andere gewissermaßen fördert“, sagt Hengel. „Wie aber die Reihenfolge ist, können wir noch nicht genau sagen.“
Virus triggert Autoantikörper-Produktion
Bei der Abwehr einer Virusinfektion werden früh Antikörper gegen das Virus gebildet, um dieses zu bekämpfen. Die veränderte Zuckersignatur auf Antikörpern führt aber dazu, dass eine ungewöhnlich starke Immunreaktion eingeleitet wird. „Bei schweren COVID-Verläufen tun diese virusspezifischen Antikörper das auf so extreme Weise, dass es hier schon zu einem massiven Gewebeschaden kommen kann“, betont Hengel. „Sie produzieren so ein entzündliches Milieu und zerstören virusinfizierte Zellen, aus denen körpereigene Moleküle frei werden.“ So bilden sich Immunkomplexe aus Virusantigenen und virusspezifischen Antikörpern. Normalerweise bauen die Makrophagen die Immunkomplexe durch Phagozytose wieder ab. Ist das Phagozytosesystem aber überfordert, lagern sich die Komplexe in Geweben ab, was andere Immunzellen auf den Plan ruft. Es kann zur lokalen Entzündung etwa in kleinen Blutgefäßen kommen, was zur Freisetzung von Selbst-Antigenen und Entzündungsmediatoren wie Zytokinen und Chemokinen führt.
Durch die Botenstoffe werden Immunzellen des adaptiven Immunsystems stimuliert, welche wiederum hochsensibel auf die neuen löslichen Immunkomplexe reagieren, die sich nun aus Selbst-Antigenen und Autoantikörpern gebildet haben. Auf spezifischen Immunzellen, den T-Zellen, taucht plötzlich ein Rezeptor aus der Familie der Fc-Rezeptoren auf, der eigentlich zum angeborenen Immunsystem gehört, Immunkomplexe bindet und auf Makrophagen normalerweise den Befehl zu ihrem Abbau gibt. Hier wird er jedoch plötzlich in seiner aktivierten Form als Signalüberträger auf den T-Zellen exprimiert, die zum adaptiven Immunsystem gehören und gibt den fatalen Befehl zur Produktion von Entzündungsmediatoren und weiteren Autoantikörpern.
Die T-Zellen erfahren dadurch eine zusätzliche Aktivierung, die ihre normale Toleranz außer Kraft setzt, eigene Zellen nicht anzugreifen. „Es ist immer ganz gefährlich, wenn viele Immunzellen auf einen Schlag aktiviert werden und sie nicht mehr ihrem ursprünglichen Befehl folgen“, sagt der Forscher. „Plötzlich werden alle T-Zellen über diesen Fc-Rezeptor gesteuert, produzieren Zytokine und entfachen so unkontrollierte Entzündung.“ Die daraus resultierende systemische Gewebeschädigung wird von den löslichen und zirkulierenden Immunkomplexen im Blut nicht nur in Gang gehalten, sondern noch verstärkt.
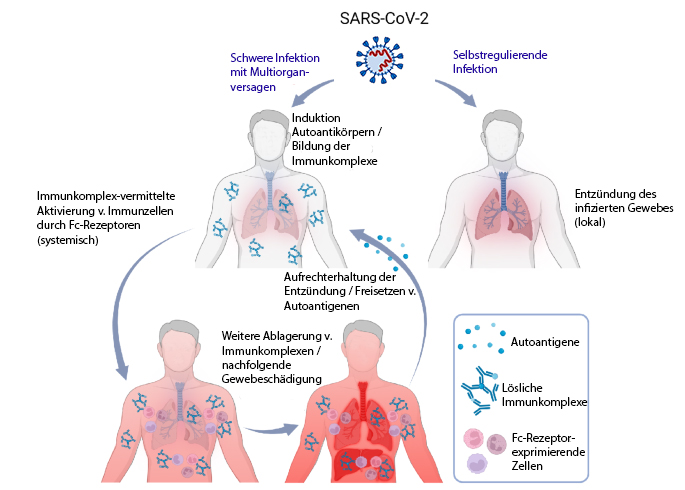 In Abhängigkeit von Prädisposition und Autoantikörperbildung kommt es zu einer schweren systemischen oder nur einer lokalen Infektion bei Covid-19.
In Abhängigkeit von Prädisposition und Autoantikörperbildung kommt es zu einer schweren systemischen oder nur einer lokalen Infektion bei Covid-19.
Quelle: Springer Nature I Philipp Kolb et al. I verändert durch S. Heyl I CC BY 4.0 https://creativecommons.org/licenses/by/4.0/
Prädisposition als zusätzlicher Faktor
Durch einen weiteren Mechanismus wird der Teufelskreis der Überreaktion noch angetrieben. Die stark aktivierten T-Zellen bewirken jetzt, dass die B-Zellen vermehrt Autoantikörper produzieren, die mit der Virusinfektion selbst nichts mehr zu tun haben. Manche Patientinnen und Patienten besitzen eine Prädisposition für ein geringes Vorkommen an Autoantikörpern, das ungefährlich ist. Wenn aber die B-Zellen übermäßig angetrieben werden, produzieren sie immer mehr dieser Antikörper, die sich dann wiederum in den Immunkomplexen finden. Wichtigster Risikofaktor für eine immunologische Entgleisung ist das Alter, denn das Immunsystem verändert sich und wird infolge der Immunseneszenz offenbar irrtumsanfälliger. Die Wirkung der Immunkomplexe erklärt die systemische Komponente der Krankheit gut und ist bei verschiedenen Autoimmunerkrankungen sehr ähnlich.
Bei Patientinnen und Patienten mit mildem Verlauf und direkt nach der Impfung wurden die Immunkomplexe nicht gefunden. Daher glauben die Forschenden, dass sie mit den löslichen Immunkomplexen einen guten Biomarker für schwere Verläufe entdeckt haben. Für eine Behandlung wäre naheliegend, die Immunkomplexe oder die Autoantikörper aus dem Plasma der Patientinnen und Patienten zu entfernen. Möglich wäre dies mit einer extrakorporalen Therapie - der allerdings aufwendigen und teuren Plasmapherese. „Man leitet das Blut heraus, separiert das Plasma, ersetzt es mit Albumin und Flüssigkeit und gibt dieses dem Patienten zurück“, erklärt Hengel. Zu befürchten ist aber, dass die Autoantikörperbildung im Körper weiter besteht und das Verfahren mehrfach wiederholt werden muss. Derweil gehört die Behandlung mit Kortison und anderen entzündungshemmenden Wirkstoffen zu den erfolgreichsten unmittelbaren Therapien.