Für den Menschen Unsichtbares sichtbar machen
KI-gestützte Bildgebung erweitert Möglichkeiten in der Chirurgie
Vor allem bei endoskopischen Eingriffen haben Ärztinnen und Ärzte häufig nur eingeschränkte Sicht auf das Operationsfeld. Ein in der Abteilung von Prof. Dr. Lena Maier-Hein am DKFZ in Heidelberg entwickeltes neuartiges Verfahren kombiniert spektrale Bildgebung mit KI-basierter Datenauswertung und erlaubt dadurch nicht nur eine präzise Gewebedifferenzierung, sondern liefert zusätzlich Echtzeit-Informationen über die Organfunktion.
„Wir wollen die Chirurgie mit Hilfe von Datenwissenschaften revolutionieren“, beschreibt Prof. Dr. Lena Maier-Hein die Mission ihrer Abteilung Intelligente Medizinische Systeme am Deutschen Krebsforschungszentrum (DKFZ) in Heidelberg. Forschende aus den Fachrichtungen Informatik, Physik, Mathematik und Statistik erarbeiten Verfahren, um chirurgische Eingriffe durch den Einsatz von maschinellem Lernen und Künstlicher Intelligenz (KI) besser und sicherer zu machen.
Insbesondere bei minimal-invasiven Operationen ist die visuelle Wahrnehmung der Behandelnden sehr begrenzt. Dies liegt unter anderem daran, dass konventionelle Endoskopkameras das menschliche Auge nachahmen und nur Licht im RGB (Rot, Grün, Blau) -Bereich erfassen. Auf diese Art und Weise ist eine präzise Gewebedifferenzierung und Beurteilung der Organfunktion allerdings kaum möglich.
Multispektrale Bildgebung liefert mehr Details
 Die von Prof. Dr. Lena Maier-Hein (a) geleitete Abteilung Intelligente Medizinische Systeme am DKFZ entwickelt KI-gestützte multi- und hyperspektrale Kamerasysteme für den Einsatz in der Chirurgie. Die Arbeitsgruppe von Dr. Alexander Seitel (b) erarbeitet zudem neuartige Verfahren der photoakustischen Bildgebung. © (a) Jutta Jung / DKFZ (b) Keno März / Alexander Seitel
Die von Prof. Dr. Lena Maier-Hein (a) geleitete Abteilung Intelligente Medizinische Systeme am DKFZ entwickelt KI-gestützte multi- und hyperspektrale Kamerasysteme für den Einsatz in der Chirurgie. Die Arbeitsgruppe von Dr. Alexander Seitel (b) erarbeitet zudem neuartige Verfahren der photoakustischen Bildgebung. © (a) Jutta Jung / DKFZ (b) Keno März / Alexander SeitelDas Team um Maier-Hein entwickelte deshalb in enger Kooperation mit Partnern am Universitätsklinikum Heidelberg ein neuartiges endoskopisches Kamerasystem, das wesentlich detailliertere Informationen über Gewebeeigenschaften liefert. Das System erfasst nicht nur elektromagnetische Strahlung im sichtbaren Bereich, sondern zusätzlich Ultraviolett- und Infrarot-Strahlung und analysiert die Daten in Echtzeit. Abhängig von der Anzahl der aufgezeichneten Spektralbänder spricht man dann von multi- (bis zu einem paar Dutzend Bänder) oder hyperspektraler (hohe Auflösung mit oft mehr als 100 Messwerten pro Pixel) Bildgebung.
„Durch die von Gewebe und Wellenlänge abhängige Reflexion und Absorption des eingestrahlten Lichts erhalten wir viele Informationen über Zusammensetzung und physiologischen Eigenschaften“, erläutert Dr. Alexander Seitel, stellvertretender Abteilungsleiter. „Jede Struktur und jedes Molekül hat individuelle optische Eigenschaften, die Rückschlüsse auf die Funktion ermöglichen können. Beispielsweise lässt sich allein anhand eines Spektralbildes beurteilen, wie gut die Sauerstoffsättigung, also die Durchblutung in bestimmten Gewebetypen ist. Dies macht die Technik besonders interessant für eine Vielzahl an klinischen Anwendungen, die wir zusammen mit unseren Partnern an den Universitätskliniken Heidelberg und Mannheim erproben.“
Visualisierung der Sauerstoffsättigung ohne Kontrastmittel
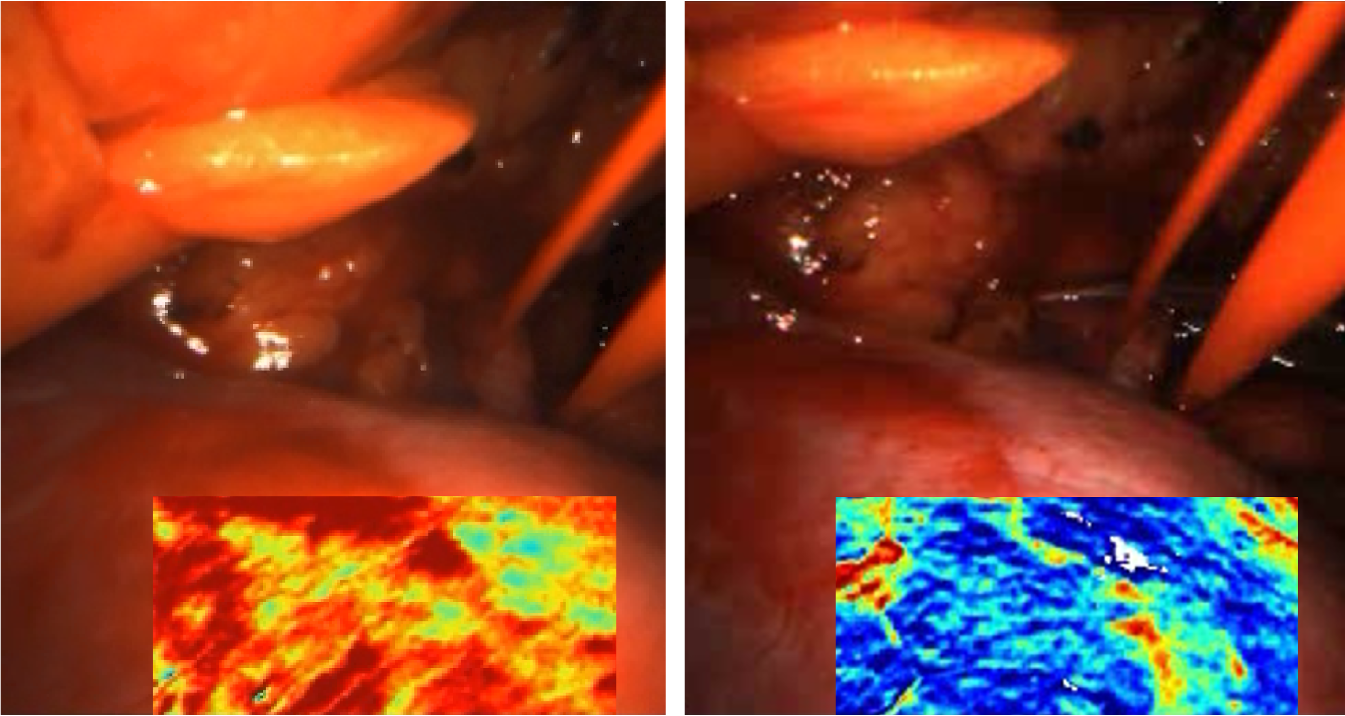 Darstellung der Sauerstoffsättigung (rot: hoch, blau: niedrig) mit Hilfe des MSI-Systems vor (links) und nach (rechts) Wiederdurchblutung der Niere während einer Operation. © Deutsches Krebsforschungszentrum (DKFZ)
Darstellung der Sauerstoffsättigung (rot: hoch, blau: niedrig) mit Hilfe des MSI-Systems vor (links) und nach (rechts) Wiederdurchblutung der Niere während einer Operation. © Deutsches Krebsforschungszentrum (DKFZ)Um übermäßige Blutungen zu verhindern, muss bei vielen Operationen der Blutfluss zu einer spezifischen Geweberegion oder einem Organ unterbunden werden. Überprüft wird das erfolgreiche Abklemmen bisher mittels intravenöser Gabe des Fluoreszenzfarbstoffes Indocyaningrün (ICG). ICG bindet innerhalb von Minuten fast vollständig an die Plasmaproteine des Blutes und ermöglicht so die Visualisierung von Gefäßen. Fehlende Fluoreszenz signalisiert dementsprechend Minderdurchblutung. Wurde allerdings die falsche Region abgeklemmt bzw. der Durchfluss nicht vollständig gestoppt, kann der ICG-Test erst nach einer etwa 30-minütigen Auswaschphase wiederholt werden. Zudem treten in seltenen Fällen schwerwiegende Unverträglichkeiten auf.
Ein bereits 2018 in der Gruppe von Maier-Hein entwickeltes MSI (Mulitspectral Imaging)-System hingegen analysiert die Sauerstoffsättigung ohne Verwendung von Kontrastmittel. Die mit einem Standardendoskop verbundene multispektrale Kamera nimmt die unterschiedlichen Absorptionsspektren von oxygeniertem und desoxygeniertem Hämoglobin auf. Mit Hilfe spezieller Deep Learning-Algorithmen können die Bilddaten (25 Bilder pro Sekunde) in Echtzeit ausgewertet werden. Da zwischen den Organen verschiedener Personen aber eine hohe Variabilität besteht, erarbeiteten die Forschenden zudem einen personalisierten Ansatz. Um eine Minderdurchblutung zu detektieren, greifen die Algorithmen nicht auf die Daten einer großen Patientenkohorte zurück, sondern nutzen als Referenz eine kurze Videosequenz, die zu Beginn der Operation von dem betroffenen Organ aufgenommen wird.
In Zusammenarbeit mit dem Städtischen Klinikum Karlsruhe (Prof. Dr. Dogu Teber) wurde das neuartige multispektrale Endoskop bereits erfolgreich bei Patientinnen und Patienten eingesetzt, die sich einer partiellen Nierenresektion unterzogen.1) Im Vergleich zur klassischen ICG-Methode lässt sich die Gewebedurchblutung genauso gut darstellen, das MSI-System bietet aber drei entscheidende Vorteile: es ist nicht-invasiv, kann mehrfach angewandt werden und erlaubt ein kontinuierliches Echtzeit-Monitoring.
Sepsisdiagnose durch HSI-Aufnahme der Hand
Ein weiteres Projekt beschäftigt sich mit der Sepsisdiagnostik. Da es bisher keine eindeutigen Biomarker für diese lebensbedrohliche Entzündungsreaktion gibt, wird sie häufig erst erkannt, wenn die Organe bereits versagen. Seit einigen Jahren kristallisiert sich allerdings heraus, dass bereits im frühen Stadium Störungen der Mikrozirkulation auftreten, die unter anderem zu kleinen Ödemen im Gewebe führen. In einer kürzlich veröffentlichten Studie nahmen die Forschenden deshalb von sämtlichen Patientinnen und Patienten der Intensivstation des Heidelberger Universitätsklinikums hyperspektrale Bilder (HSI) der Handfläche und des Ringfingers auf. 2) Mit Hilfe von Deep Learning-Algorithmen analysierten sie die Bilddaten bezüglich Sauerstoffsättigung, Durchblutung und Hämoglobin- sowie Wassergehalt und konnten zeigen, dass auf diesem Weg eine zuverlässigere Sepsisdiagnose und auch Sterblichkeitsvorhersage als mit gängigen Tests möglich ist. Die HSI-Analyse stellt somit ein schnelles, nicht-invasives, mobiles und kostensparendes Verfahren dar. Damit wäre es als Pre-Screening-Tool zur Identifizierung von Personen geeignet, bei denen weiterführende Untersuchungen notwendig sind.
Photoakustische Bildgebung für tieferen Blick ins Gewebe
Da MSI und HSI nur Daten von Oberflächen erfassen können, nutzt die von Medizininformatiker Seitel geleitete Gruppe eine andere Aufnahmetechnologie: die photoakustische Bildgebung. Hierbei werden kurze Lichtpulse ins Gewebe gesendet und dort von Molekülen und Strukturen absorbiert. Dies führt zu lokaler Erwärmung und Ausdehnung, wodurch kleine Schockwellen entstehen, die sich mit Hilfe von Ultraschallsensoren detektieren lassen. Der Wissenschaftler führt aus: „Auf diese Weise können multispektrale dreidimensionale Bilder aus Gewebeschichten in mehreren Zentimetern Tiefe generiert werden. Da das Licht auf dem Weg dorthin aber abgeschwächt wird, ist es komplizierter, Rückschlüsse auf die Konzentration der detektierten Substanzen zu ziehen. Die klinische Anwendung der photoakustischen Bildgebung ist deshalb noch nicht so weit fortgeschritten. Prinzipiell kann aber auch mit dieser Technologie beispielsweise die Sauerstoffsättigung bestimmt werden.
Des Weiteren erarbeitet die Abteilung Intelligente Medizinische Systeme generelle Ansätze zur Anwendung von KI in der Chirurgie, beispielsweise um Bilddaten auszuwerten. Außerdem werden sogenannte Foundation Models (Grundmodelle) entwickelt, die für verschiedene Fragestellungen geeignet sind. „Wir wollen weg von dem subjektiven Wissen, das nur wenige erfahrene Chirurgen im Laufe der Zeit angesammelt haben, hin zu einem Kollektivwissen, das mit Hilfe der KI aus Millionen Fällen mit bekanntem Outcome generiert werden kann“, schildert Maier-Hein, die auch geschäftsführendes Direktoriumsmitglied am Nationalen Centrum für Tumorerkrankungen (NCT) ist, den Hintergrund der Forschungsprojekte.
Ein weiterer Schwerpunkt liegt auf der Validierung der KI-basierten Lösungen. Damit die Ergebnisse verlässlich zur Problemstellung passen, müssen genügend Daten und die richtigen Metriken verwendet werden. Um zu klären, wie sich die Güte von Algorithmen in der medizinischen Bildverarbeitung bestimmen lässt, wurde ein großes Expertenkonsortium mit internationaler Beteiligung gebildet. Auf Basis einer systematischen iterativen Befragung erarbeitete das Kernteam in Heidelberg dann Empfehlungen für die Entwicklung KI-unterstützter Verfahren, an denen sich andere Forschende orientieren können.
Insgesamt zielen alle Anstrengungen darauf ab, die Chirurgie durch verbesserte Bildgebung sicherer zu machen. Für die innovativen Arbeiten in ihrer Abteilung wurde Maier-Hein 2024 mit dem Deutschen Krebspreis für Translationale Forschung sowie dem Landesforschungspreis Baden-Württemberg ausgezeichnet.