AaviGen GmbH: Hoffnung bei Herzinsuffizienz
Gentherapie für geschwächte Herzen
Ein schwaches Herz – etwa nach einem Infarkt – beim Hausarzt mit einer einmaligen intravenösen Injektion therapieren, und dies auch noch ohne ernsthafte Nebenwirkungen: Was sich fast zu schön anhört, um wahr zu sein, ist tatsächlich bereits in der Entwicklung. Das Heidelberger Biotechunternehmen AaviGen arbeitet an einer auf Adeno-assoziierten Viren basierten Plattformtechnologie, mit deren Hilfe therapeutische Gene hochspezifisch in erkrankte Herzmuskelzellen gebracht werden können, um dort ihre heilende Wirkung zu entfalten.
Ein gesundes Herz sorgt dafür, dass unser Körper für seine Aufgaben jederzeit ausreichend mit Sauerstoff versorgt ist – und wir uns leistungsfähig und fit fühlen. Kann dieses so zentrale Organ seiner Aufgabe allerdings nur noch eingeschränkt nachkommen, so spricht man von Herzinsuffizienz. Die Gründe können unterschiedlich sein, etwa aus jahrelangem Bluthochdruck oder einem Herzinfarkt resultieren. Eine solche „Pumpschwäche“ betrifft alleine in Deutschland sehr viele: mehrere Millionen Menschen – Tendenz steigend, wie auch in allen anderen Industrieländern.1)
Ist die Diagnose Herzinsuffizienz einmal gestellt, so liegt die 5-Jahres-Überlebensrate bei nur etwa 50 Prozent, denn die derzeitigen Behandlungsmöglichkeiten sind mehr als begrenzt: Die einzige ursächliche Therapie ist eine Herztransplantation, die für weniger als 0,001 Prozent aller Erkrankten infrage kommt. Für alle anderen bleibt lediglich die Behandlung der Symptome.2)
Interdisziplinäres Team aus Gentherapie-Pionieren und Gründungsexperten
 Prof. Dr. Patrick Most ist Mitgründer der AaviGen – einem jungen Biotechunternehmen, das heilende Gentherapien für Herz-Kreislauferkrankungen entwickelt. © AaviGen
Prof. Dr. Patrick Most ist Mitgründer der AaviGen – einem jungen Biotechunternehmen, das heilende Gentherapien für Herz-Kreislauferkrankungen entwickelt. © AaviGenNun ist Hoffnung in Sicht: Das Biotechunternehmen AaviGen GmbH aus Heidelberg entwickelt kleinste, herzspezifische, synthetische virale „Universaltaxis“, die therapeutische Gene gezielt an den Ort des Geschehens bringen und Herzzellen unterstützen oder heilen könnten. Dabei kann das Start-up auf langjährige Expertise bei der Entwicklung von heilenden Gentherapien für Herz-Kreislauf-Erkrankungen zurückgreifen: Prof. Dr. Patrick Most, einer der Firmengründer, CEO und gleichzeitig Leiter der Sektion Molekulare und Translationale Kardiologie an der Abteilung für Kardiologie des Universitätsklinikums Heidelberg, forscht seit Langem auf diesem Gebiet. Er gründete bereits 2014 zusammen mit Prof. Dr. Hugo Katus die InoCard GmbH, die mit einer Gentherapie für Herzmuskelschwäche der ersten Generation Teil des niederländischen Gentherapie-Spezialisten uniQure wurde.
Das Führungsteam der AaviGen umfasst außer Most noch drei weitere Mitgründer: Prof. Dr. Hugo Katus, CMO und international führender Experte für Herz- und Kreislaufmedizin durch langjährige Tätigkeit als ärztlicher Direktor der Abteilung für Kardiologie des Universitätsklinikums Heidelberg, Prof. Dr. Marc Lerchenmüller, CFO und Finanzökonom mit Spezialisierung Gesundheitswesen durch langjährige Erfahrung bei der Boston Consulting Group New York, sowie Dr. Martin Busch, COO und als biotechnologischer Experte unter anderem verantwortlich für Produktionsprozesse. Finanziert wird das junge Unternehmen derzeit über eine Beteiligung von Dietmar Hopp.
Herzspezifische rekombinante AAVs als Universaltaxis zum Herzen
„Während das Prinzip der Gentherapie vor Jahrzehnten in der Akademie entwickelt wurde und sich das enorme therapeutische Potenzial bereits in der erfolgreichen Zulassung von Gentherapeutika in den USA und Europa dokumentiert, ist für den Herzpatienten bisher nichts in der Klinik angekommen“, erklärt Most. „Grund hierfür ist nicht, dass es keine therapeutischen Gene gäbe, die Krankheiten des Herzmuskels heilen könnten, sondern dass es bisher nicht möglich ist, diese in wirksamer Dosis und einfacher Form an Ort und Stelle zu bekommen. Unser Ziel ist es, dies zum Wohle der Patienten grundlegend zu ändern. Mit der technologischen AaviGen-Plattform entwickeln wir synthetische Genfähren, mit deren Hilfe wir therapeutische Gene personalisiert, sicher, einfach und präzise in den erkrankten Herzmuskel transportieren und platzieren können. Konkret konzentrieren wir uns derzeit auf die Entwicklung von Gentherapien für kardiovaskuläre und kardiopulmonale Erkrankungen – sowohl für im Lauf des Lebens erworbene als auch angeborene, das heißt genetisch bedingte Herzleiden.“
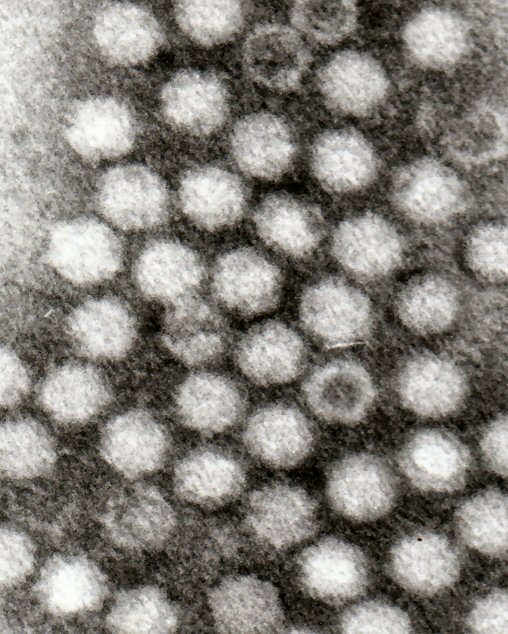 Als Genfähren für die therapeutischen Sequenzen zum Herzen verwendet die AaviGen Adeno-assoziierte Viren (AAVs). Quelle: Dr Graham Beards, Wikipedia, CC BY-SA 3.0, https://creativecommons.org/licenses/by-sa/3.0/deed.en
Als Genfähren für die therapeutischen Sequenzen zum Herzen verwendet die AaviGen Adeno-assoziierte Viren (AAVs). Quelle: Dr Graham Beards, Wikipedia, CC BY-SA 3.0, https://creativecommons.org/licenses/by-sa/3.0/deed.enMit dem ersten Produkt in einer Klinischen Studie rechnet der Experte in sechs bis sieben Jahren: „Wir stehen am Anfang einer herausfordernden Aufgabe, aber wir sehen am internationalen Wettbewerb um uns herum schon jetzt: Wir sind mit unseren Alleinstellungsmerkmalen richtig positioniert. Es gibt unter anderem reges Interesse an unserer Arbeit seitens großer biopharmazeutischer Unternehmen.“
Als Genfähren nutzt AaviGen rekombinante Adeno-assoziierte Viren (AAV), in die die therapeutischen Genkassetten integriert werden, so genannte AAV-Kapside. Synthetische Spielarten dieser AAVs entwickelt das Forschungsteam über biotechnologische Verfahren: „Wir modifizieren die AAV-Oberflächen genetisch und molekular so, dass sie letztlich einen hohen kardialen Tropismus [Anm. d. Red.: Tropismus bezeichnet die Eigenschaft eines Virus einen bestimmten Zelltyp zu infizieren und sich dort zu vermehren] aufweisen und damit die therapeutischen Genkassetten präzise und zuverlässig in Herzmuskelzellen einbringen können“, erklärt Most. „Dies ermöglichst es, die Behandlung in Zukunft einmal bei jedem niedergelassenen Hausarzt durchzuführen. Hierzu sehen wir lediglich eine einfache intravenöse Injektion voraus, deren Wirkung mehrere Jahre anhalten kann – vielleicht sogar auch lebenslang.
Der exklusive kardiale Vektortropismus hat außerdem auch noch einen zweiten wichtigen Aspekt: Dadurch, dass die Genfähren wirklich nur auf Herzmuskelzellen fixiert sind und z. B. die Leber als wichtigsten Auslöser unerwünschter Wirkungen von Gentherapien umgehen, wird man unsere Gentherapeutika wesentlich niedriger dosieren können, was natürlich weniger Nebenwirkungen mit sich bringt. Das bedeutet eine radikale Vereinfachung des ganzen Systems.“
Infobox: Adeno-assoziierte Viren (AAV)
Bei den AAV handelt es sich um eine Virusart, die ohne Helfer – ein Adenovirus –, der dieselbe Zelle befällt, nicht auskommt. Sie werden gerne als virale Vektoren für Gentherapien verwendet, weil sie keine Krankheitsüberträger sind, dafür stabiler als Adenoviren alleine, aber genauso spezifisch bestimmte Zelltypen infizieren. Von Nachteil für diese Anwendung ist allerdings ihr relativ kleines Genom.
Aus bestimmten, natürlich vorkommenden AAV-Varianten werden bei der AaviGen synthetische Varianten geschaffen, die nach Injektion vollständig zum Herzen gelangen, nicht etwa auch zur Leber, wie dies bei anderen Arzneimitteln der Fall ist. Durch diese große Spezifität kann die Dosis gering gehalten werden. Und da die AAV in der Leber keine Toxizität mehr entwickeln können, wird auch mit keinen nennenswerten Nebenwirkungen gerechnet.
Der Nachteil des begrenzten Genoms, das zur Verpackung der therapeutischen Sequenzen zur Verfügung steht, wird entweder in Kauf genommen und damit das Target so klein gehalten, dass es in den AAV-Partikel passt. Man spricht dann von einer Genaddition – also einer zusätzlichen Kopienzahl bestimmter Gensequenzen im Herzmuskel. Falls dies nicht möglich ist, kann die Mini-CRISPR/Cas-Methode zum Einsatz kommen, bei der die therapeutischen Genkassetten durch Genedition verpackt werden.
Gentherapie stärkt noch verbliebene gesunde Herzmuskelzellen
In den Herzmuskelzellen angekommen, werden die therapeutischen Gene freigesetzt und exprimiert. Im Fall einer Postinfarkt-Herzmuskelschwäche besteht die Wirkung beispielsweise darin, dass der noch verbliebene, funktionstüchtige Restmuskel durch die Gentherapie gestärkt wird, sodass der durch die Erkrankung erlittene Verlust an Herzgewebe ausgeglichen werden kann.
In der Planung haben die Heidelberger Forschenden letztlich ein Portfolio aus mehreren AAV-Kapsiden, alle spezifisch für Herzmuskelzellen, die aber auf unterschiedliche Herzerkrankungen abzielen und personalisierte Therapien ermöglichen sollen: „Je nach Erfordernissen des therapeutischen Gens bzw. der Indikation kann ein Herz-AAV-Vektor mit den passenden Eigenschaften ausgesucht werden“, sagt der Professor. Derzeit testet man Bibliotheken aus Milliarden von Sequenzvarianten. Ebenfalls eine Innovation: Normalerweise werden derartige Entwicklungen in Zellen gestartet. Dies funktioniert dann aber nur in den seltensten Fällen in Tiermodellen, die seitens der Gesundheitsbehörden für die Gentherapieentwicklung vorgeschrieben sind. „Wir drehen diesen Prozess um und entwickeln direkt in Tiermodellen, die für die Sicherheit und Wirkung im Menschen die höchste Relevanz aufweisen“, so Most.
Aber nicht nur die Fähigkeit, zum Herzen zu gelangen, entscheidet für die Eignung einer Variante. „Sie muss sich für die Versorgung der hohen Zahl an Herzpatienten auch gut produzieren lassen“, betont der Mediziner. „Das haben wir aus vorausgegangenen Projekten gelernt, wie wichtig es ist, dies frühzeitig zu adressieren. Deshalb interagieren wir auch heute schon mit Herstellern von AAV-basierten Gentherapeutika, um die komplexen Produktionsprozesse vorzubereiten. Selbstverständlich muss in den eng abgestimmten Entwicklungsprozessen mit den Zulassungsbehörden auch sichergestellt werden, dass eine gewählte Variante sicher ist.“ Von selbst können sich diese Viren nicht mehr vermehren - weder in Körperzellen noch in der Natur -, da sie rekombinant sind und ihnen diese Fähigkeit genommen wurde.
Land Baden-Württemberg und Universität als Paten für Start-ups
Für das junge Unternehmen war neben dem überzeugten Engagement durch Dietmar Hopp auch die Unterstützung durch die Universität Heidelberg maßgeblich. „Insbesondere Prof. Eitel, Rektor der Uni, war auch bereits bei unserem ersten Start-up davon überzeugt, dass es möglich ist, akademische Innovationen erfolgreich in die bioindustrielle Translation und damit letztlich zum Patienten zu bringen“, so Most. „Und hat durch die Bereitstellung erforderlicher Beschäftigungsmodelle nicht zuletzt das innovative Konzept des akademischen Intrapreneurship am Standort sehr gefördert.“ Und auch die Unterstützung des Landes hebt Most besonders hervor: „Baden-Württemberg hat sozusagen Pate gestanden für unser Unternehmen, denn seine Translationsprogramme im Rahmen des Forums Gesundheitsstandort Baden-Württemberg haben ganz wesentlich zu unserer Entscheidung beigetragen, die AaviGen zu gründen.“