KI-gestütze Bilderkennung beschleunigt Identifizierung von Zebrafischmutanten
EmbryoNet AI identifiziert selbstständig Entwicklungsstörungen
Die embryonale Entwicklung ist bei komplexen Organismen über Signalwege genau reguliert. Bei Störung dieser Signalwege entstehen charakteristische phänotypische Entwicklungsschäden, die nicht immer leicht zu erkennen sind. Der Entwicklungsbiologe Prof. Dr. Patrick Müller hat mit der Software EmbryoNet an der Universität Konstanz ein Tool entwickelt, mit der sich Entwicklungsstörungen zuverlässig per Bildanalyse identifizieren lassen.
In der Embryogenese des Zebrafischs vom Ei zum komplexen Organismus orchestrieren evolutionär konservierte Signalwege die Bildung des Körperbaus auf vielschichtige Art. Eine Handvoll Signalwege steuert in der frühen Entwicklung das Gewebewachstum, die Differenzierung der Zellen sowie die Morphogenese, also die Bildung von Organen und Körperstrukturen, wie ein gut abgestimmter Tanz. Aus einem scheinbar unsortierten Zellhaufen entstehen Muster, daraus entwickeln sich die Achsen des Embryos, die Segmentierung und die Ausprägung der Körperteile. Die Signalmoleküle, die für die Choreografie des „Tanzes“ verantwortlich sind, weisen den noch unreifen Zellen ihren Platz zu und sorgen dafür, dass sie bei der Entwicklung vorgesehene Eigenschaften annehmen.
Zellen „wissen“, wohin sie gehören
 Prof. Dr. Patrick Müller entwickelt mit seinem Team an der Uni Konstanz ein KI-gestütztes Werkzeug, mit dem sich Embryonen und Organoide automatisiert charakterisieren lassen. © Inka Reiter
Prof. Dr. Patrick Müller entwickelt mit seinem Team an der Uni Konstanz ein KI-gestütztes Werkzeug, mit dem sich Embryonen und Organoide automatisiert charakterisieren lassen. © Inka ReiterSignalwege interagieren in komplexen Netzwerken miteinander und beeinflussen sich gegenseitig, um die sich differenzierenden Zellen zu dreidimensionalen Strukturen anzuordnen. Der Funktionsverlust eines jeden Signalwegs führt zu charakteristischen Defekten in der Musterbildung und somit in der Gestalt des Embryos. Der Entwicklungsbiologe Prof. Dr. Patrick Müller von der Universität Konstanz analysiert solche Gestaltveränderungen bei Wirbeltieren, wie beispielsweise Zebrafischen, und schlüsselt anhand der Mutanten auf, welche zugrundeliegenden Signalwege möglicherweise gestört sind. „Wenn man die Genregulation verändert, indem man die Signalmoleküle beeinflusst, bekommt man charakteristische Gestaltänderungen, die im Embryo mal offensichtlich und mal subtil sind“, sagt er. Daher ist die Charakterisierung durch Bildanalyse nicht immer eindeutig und Rückschlüsse manchmal schwierig. Seine Idee: Die Charakterisierung der Embryonen mit Hilfe von Künstlicher Intelligenz zu standardisieren, sodass eine Analyse auch im Hochdurchsatzverfahren möglich ist.„Dafür schauten wir uns einen Satz von konservierten Signalmolekülen an, die während der frühen Entwicklung angeschaltet werden, und die beim erwachsenen Tier, aber auch bei Krankheitszuständen, immer wieder verwendet werden“, erklärt der Biologe. Mit einem effizienten Werkzeug, das den Embryo analysieren kann, lassen sich zum Beispiel auch Wirkmechanismen von Substanzen und damit deren Risikobewertung auf die biologische Entwicklung leichter aufklären.
KI als Schlüsselkomponente
 Künstliche Intelligenz und Biologie: Eine Visualisierung der wissenschaftlichen Forschung, die die Entwicklung der EmbryoNet AI-Plattform vorantreibt. © Anton Startsev mit MidJourney
Künstliche Intelligenz und Biologie: Eine Visualisierung der wissenschaftlichen Forschung, die die Entwicklung der EmbryoNet AI-Plattform vorantreibt. © Anton Startsev mit MidJourneyDamit Entwicklungsstörungen beim Embryo anhand des Bildmaterials sicher klassifiziert werden können, bezieht die von Müller und seinem Team entwickelte Software EmbryoNet neben visuellen Informationen auch zeitliche Daten mit ein. Durch die Nutzung von Zeitreihen wird die Präzision nochmals deutlich verbessert. „Hier können wir dann auch die Dynamik herauslesen“, sagt Müller. „Ob etwa das normale Entwicklungstempo eingehalten wird oder es zu Verzögerungen kommt.“
Mehr als 15 Mio. Bilder haben dafür Eingang in die Künstliche Intelligenz gefunden, mehrere Terabyte an Bildmaterial, das die Forschenden eingearbeitet haben. Zentrales Element ist das im EmbryoNet enthaltene Convolutional Neural Network, ein sogenannes tiefes neuronales Faltungsnetzwerk mit verschiedenen Ebenen, die unterschiedliche Filter und Fokuspunkte haben und wechselseitig miteinander kommunizieren. „Am Ende des Netzwerks steht die Klassifizierung. Solche Netzwerke wurden von echten Gehirnprozessen inspiriert und sind ihnen sehr ähnlich“, meint Müller. Im Jahr 2023 wurde diese Methode erstmals in der Zeitschrift Nature Methods veröffentlicht und im Rahmen der 'Methode des Jahres' herausgestellt1).
Präzision und Schnelligkeit unschlagbar
Gegenüber der menschlichen Aufmerksamkeit ist EmbryoNet unvoreingenommener und robuster in der Identifizierung von Zebrafischmutanten. Außerdem arbeitet es um ein Vielfaches schneller: Während das Tool mehrere hundert Bilder in wenigen Millisekunden analysiert, brauchen Menschen einige Tage für den gleichen Datensatz, wobei die erreichte Präzision durch die KI bei unschlagbaren 90 Prozent für die korrekte Klassifizierung liegt. Erfahrene Entwicklungsbiologen erreichen 80 und eingearbeitete Studierende nur 50 Prozent. Zudem ist das System auf andere Wirbeltierarten sowie Organoide übertragbar und stellt einen wertvollen Beitrag zur tierversuchsfreien Forschung dar. Insgesamt führt dies zu einer erheblichen Steigerung der Forschungseffizienz, da EmbryoNet Phänotypen bereits Stunden vor dem menschlichen Auge in der Embryonalentwicklung erkennt und auch unvollständige Penetranz anzeigt. „EmbryoNet schaut offenbar auf Regionen, die uns bisher verborgen waren. Dadurch eröffnet sich uns eine neue Biologie, die uns vorher unbekannt war“, so Müller.
Maßgeschneiderte Lösung für Pharma und Forschung
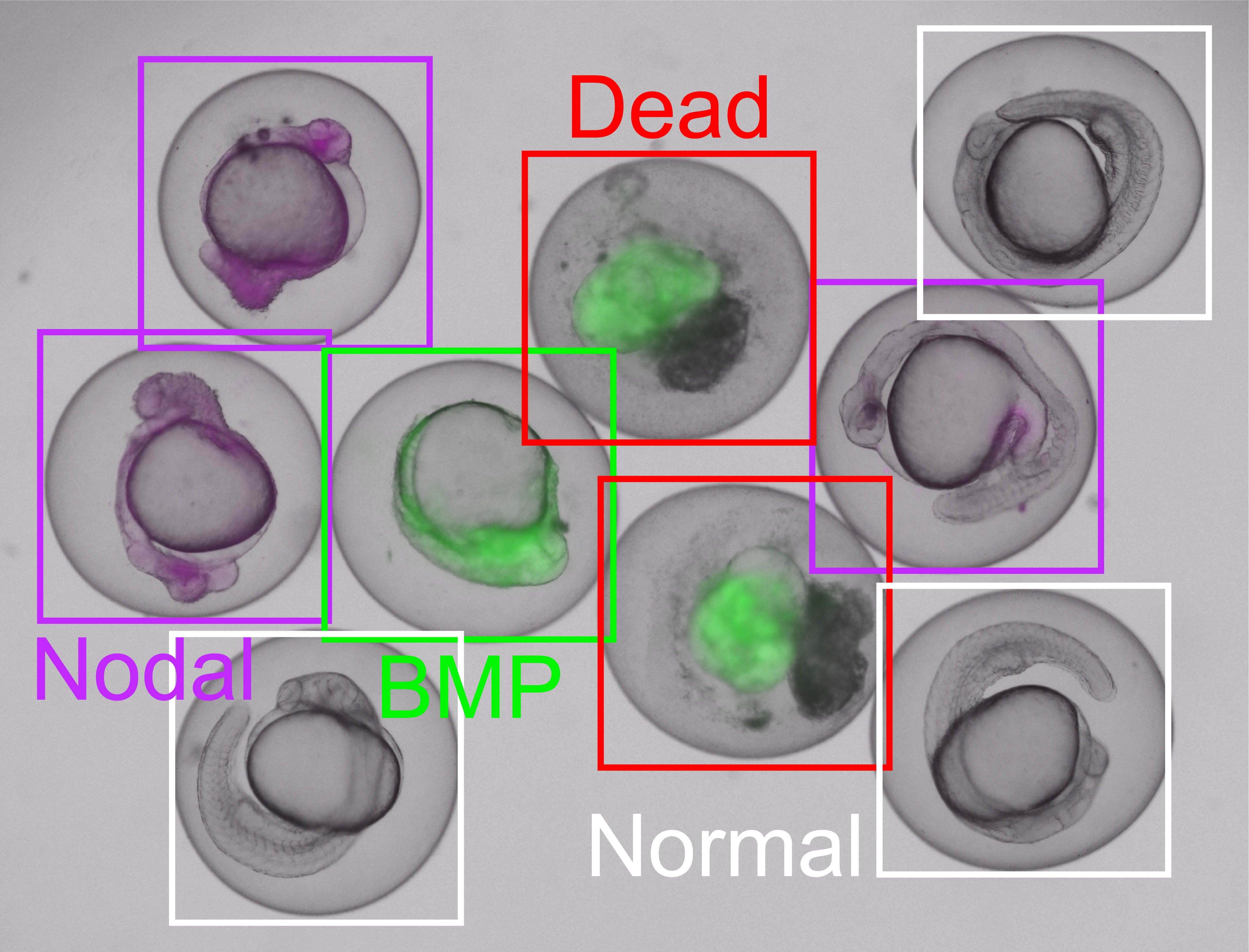 Entwicklungsstörungen können - wie hier beim Zebrafisch - zuverlässig erkannt und den zugrundeliegenden Signalwegen (nodal, BMP) zugeordnet werden. Ebenso benennt EmbryoNet normal entwickelte sowie tote Embryonen. © EmbryoNet AI
Entwicklungsstörungen können - wie hier beim Zebrafisch - zuverlässig erkannt und den zugrundeliegenden Signalwegen (nodal, BMP) zugeordnet werden. Ebenso benennt EmbryoNet normal entwickelte sowie tote Embryonen. © EmbryoNet AIBereits bekannte Medikamente lassen sich auf diese Art mit noch unbekannten Auswirkungen auf Signalwege verknüpfen. Im Wirkstoffscreen mit EmbryoNet fand Müllers Team beispielsweise heraus, dass Statine, die in verschiedenen Medikamenten zur Senkung des Cholesterinspiegels enthalten sind, einen Effekt auf die Embryogenese haben: „Die Embryonen sind in einer speziellen Weise deformiert – mit einer verkürzten Achse –, wie es charakteristisch für den FGF-Signalweg ist. Wir sehen also nicht nur, dass die Embryogenese falsch läuft, sondern sogar, was genau falsch läuft. Nämlich die FGF-Signaltransduktion“, sagt Müller. „Dieser Signalweg ist nicht nur wichtig für die Embryogenese, er wird auch oft später in Krebszellen fehlreguliert.“ Müllers Hoffnung ist, „dass man mit Antagonisten zukünftig gegenlenken könnte, um Defekte eventuell in die andere Richtung zu beeinflussen.“
Mit seinem Start-up EmbryoNet AI Technologies möchte Müller diese Innovationen nun für die pharmazeutische Industrie nutzbar machen. Er verspricht eine einfache Handhabung als Web-Anwendung, für die keine spezielle Expertise nötig ist: „Ein Bild, das man im Labor aufgenommen hat, zieht man per Drag and Drop in seinen Browser und bekommt sofort die Analyse. Man sieht, um welchen Phänotyp es sich handelt, welche Morphologie gestört ist, welche Gewebezusammensetzung wir haben und vieles mehr.“ Zehn Bilder können anfangs kostenlos analysiert werden, um zu kontrollieren, ob EmbryoNet AI funktioniert. Danach können jährliche Lizenzen - sogar zusammen mit einem Hochdurchsatzmikroskop - erworben werden. Für den Forschungstransfer dieser Technologie erhielt das Start-up den Gründungspreis 2025 vom Bundesministerium für Wissenschaft und Klimaschutz (BMWK) sowie einen Proof of Concept Grant des Europäischen Forschungsrats.
Während Müller und sein Team daran arbeiten, eine regulatorische Zulassung bei der Europäischen Arzneimittelagentur (EMA) zu bekommen, hofft er, mit EmbryoNet AI einen standardisierten Beitrag für die Forschung zu leisten, der gleichzeitig eine höhere Aussagekraft für die humane Biologie liefert.