Tödlich, unheilbar und meist zu spät erkannt - Bauchspeicheldrüsenkrebs ist bald die zweithäufigste Todesursache bei Krebs, die Inzidenz steigt. Was macht diesen Tumor zu einer solch großen Herausforderung für die Medizin?
Die Verläufe sind so heterogen, dass fast jede Patientin und jeder Patient eine eigene Erkrankung und die Vergleichbarkeit nicht groß ist. Da gibt es riesige Unterschiede, deren Gründe nur zum Teil klar sind. Vieles wird von den molekularen Veränderungen im Tumor bestimmt, vieles auch von der unmittelbaren Tumorumgebung. Beim Pankreaskarzinom hat das Immunsystem aktuell keine Chance, weil der Tumor sehr viele Faktoren herstellt, die das Immunsystem abschalten, sodass diese Unterstützung, die in vielen Fällen durch neue Immuntherapien immer besser möglich ist, bislang nicht zum Tragen kommt.
 UNITEPANC-Studienleiter Prof. Dr. Thomas Seufferlein, Ärztlicher Direktor Klinik für Innere Medizin I am Universitätsklinikum Ulm © Universitätsklinikum Ulm
UNITEPANC-Studienleiter Prof. Dr. Thomas Seufferlein, Ärztlicher Direktor Klinik für Innere Medizin I am Universitätsklinikum Ulm © Universitätsklinikum UlmSie sind seit mehr als zwei Jahrzehnten als Mediziner und Forscher in diesem Feld tätig. Gab und gibt es Fortschritt in Diagnose und Therapie dieser Erkrankung?
Wir haben die Überlebenszeiten deutlich verlängert. Im Jahr 2000 lagen sie im Mittel bei zwei Jahren, mittlerweile nach der Operation bei 54 Monaten. In der Früherkennung der Erkrankung haben wir wenig Fortschritte gemacht, und bei metastasierten Patientinnen und Patienten liegt die Überlebenszeit gerade mal bei elf bis zwölf Monaten. Jetzt sehen wir tatsächlich eine neue Gruppe von Wirkstoffen, RAS-Inhibitoren [Anm. d. Red.: 80 Prozent der Tumoren haben RAS-Veränderungen].
In den letzten drei, vier Jahren gelang es, effektive Inhibitoren gegen mutiertes RAS herzustellen. Diese Substanzen verändern möglicherweise die Therapielandschaft beim Pankreaskarzinom nachhaltig. Eine große Studie, an der wir auch beteiligt waren, wurde gerade abgeschlossen (NCT06625320). Die Ergebnisse werden mit Spannung erwartet, weil wir erstmals eine der Schlüsselmutationen des Tumors attackieren können.
Was sind das für neue Wirkstoffe?
Es handelt sich um Inhibitoren von RAS, die entweder ganz spezifische Mutationen in RAS-Proteinen selektiv adressieren oder bei PAN-RAS-Inhibitoren global wirken - je nach Auswahl mit unterschiedlichem Wirkprofil und mit jeweils unterschiedlichem Nebenwirkungsprofil. Das geht so weit, dass PAN-Inhibitoren nicht nur das mutierte, sondern auch das endogene RAS-Molekül hemmen, was die Nebenwirkungen erhöht, weil zum Beispiel auch Stammzellen im Darm RAS für die Differenzierung brauchen.
Welche Ziele verfolgt UNITEPANC?
Im Grunde sind es zwei Ziele. Wir versuchen, die unterstützende Chemotherapie nach einer Pankreaskarzinom- OP zu verbessern. Deshalb generieren wir aus dem Tumor des Patienten oder der Patientin, der bei der OP entnommen wird, Minitumoren, sogenannte Organoide, behandeln diese patientenindividuell mit den Chemotherapeutika und überprüfen deren Empfindlichkeit bzw. Resistenz auf die entsprechende Substanz.
Das andere Ziel unserer Phase-I-Studie ist es zu zeigen, dass dieses Verfahren an mehreren Standorten funktioniert und so robust ist, dass es in der Versorgung einsetzbar ist.
Warum ist das so schwierig?
Es ist ein hochkomplexes Verfahren, das sehr störanfällig sein kann. Wir führten zwei Jahre lang Ringversuche an unterschiedlichen Standorten durch. Jetzt wollen wir prüfen, ob das im klinischen Setting machbar ist. Die Frage ist: Kann man die Organoid-Herstellung dezentralisieren, oder muss man zentralisieren, falls es das in die Klinik schafft?
Wie lässt sich der Nutzen für die Patientinnen und Patienten beschreiben?
Wenn wir herausfinden, dass ein Patient oder eine Patientin eigentlich die Maximaltherapie vertragen könnte, sich aber laut Organoid-Befund mit einer viel weniger aggressiven Therapie genauso gut behandeln lässt, dann hätte man ihm viel Toxizität erspart, was mit deutlich weniger Belastung einhergeht.
UNITEPANC ist weltweit die erste multizentrische Studie?
Der Superlativ bezieht sich darauf, dass es bislang niemand multizentrisch als prospektiv randomisierte kontrollierte Studie versucht hat – die meisten machen es umgekehrt: Sie machen eine Studie und gewinnen im Rahmen der Studie auch Organoide. Dass man eine multizentrische Studie macht, aus deren Ergebnissen sich eine Entscheidung ableitet, das gab es bislang nicht, weil es schwierig ist. Wir wollen tatsächlich den Lackmus-Test machen: Schafft es diese Technik in die Klinik?
Wie groß ist der Anteil derjenigen Patientinnen und Patienten, für die eine OP überhaupt in Frage kommt?
20 Prozent, nicht mehr.
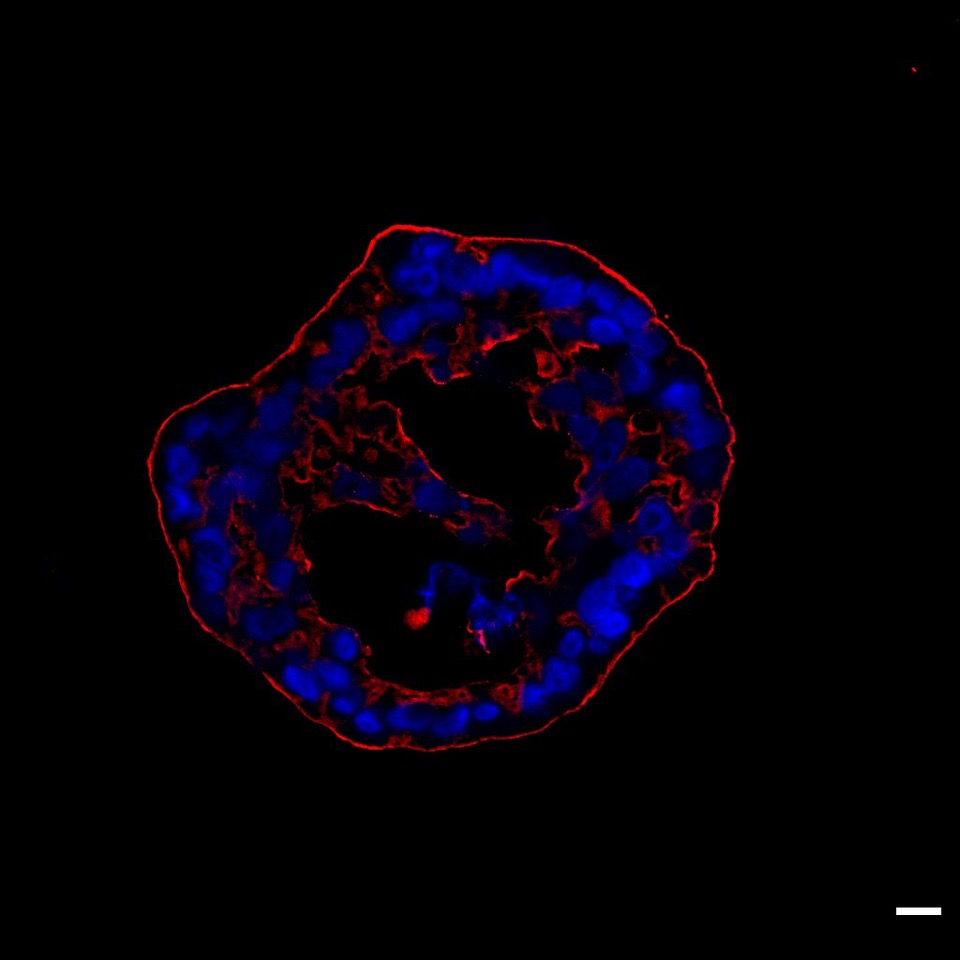 Schaffen es Organoide in die Klinik? Unser Bild zeigt ein patientenabgeleitetes immunfluoreszierendes Organoid. © IMOS, Prof. Alexander Kleger, Uniklinikum Ulm
Schaffen es Organoide in die Klinik? Unser Bild zeigt ein patientenabgeleitetes immunfluoreszierendes Organoid. © IMOS, Prof. Alexander Kleger, Uniklinikum UlmDas ist im Grunde ein bescheidenes Ziel...
Das ist eines der wesentlichen Probleme dieser Erkrankung: Uns fehlen Diagnostika für die Früherkennung. Das Pankreaskarzinom ist ein Tumor, der sehr wenig Tumormaterial ins Blut abgibt, und sich im Blut in frühen Stadien schlecht nachweisen lässt. Alle Symptome sind unspezifisch. Viele Patientinnen und Patienten in höherem Lebensalter (6. - 8. Lebensjahrzehnt) werden wegen Rückenschmerzen behandelt, bis sich herausstellt, dass ein Pankreastumor entlang der Nervenscheiden wächst. Das projiziert der Kopf in den Rücken, kommt aber eigentlich von einem Bauchspeicheldrüsentumor.
Auch sehr gute Bildgebung ist noch nicht perfekt und kann Frühformen nur sehr bedingt und in Einzelfällen erkennen.
Klingt so, als ob die Frühdiagnose weiterhin schwierig bleibt.
Das ist absolut schwierig und eine große Herausforderung für die Forschung. Auch hier spielen RAS-Mutationen eine Rolle, die frühe Veränderungen bei der Entstehung von Pankreaskarzinomen darstellen. Das Problem ist nur: Diese Veränderungen können, müssen aber nicht einen Tumor auslösen. Bei Autopsie-Studien sieht man, dass etliche Menschen Tumorvorstufen im Pankreas haben, aber kein Karzinom entwickelt haben.
Gibt es bereits eine Organoid-Technologie, die es erlaubt, überall tumorbasierte Organoide nach demselben Verfahren herzustellen, sie vergleichbar und mithin reproduzierbar zu machen?
Es gibt tatsächlich Ansätze von Firmen, das zu standardisieren. Aber von diesen Firmen habe ich noch keine prospektive Studie gesehen, um den Ansatz zu validieren. Das bewegt sich alles auf Forschungsebene.
Ist die intratumorale Heterogenität eines Primärtumors in diesen Avataren gewährleistet wie in vivo?
Das Tumormikromilieu fehlt, z. B. tumorassoziierte Bindegewebszellen, Makrophagen, Kollagen und Stroma. Trotzdem sind die Korrelationen der Ergebnisse zwischen Organoid und Patientin oder Patient in unseren retrospektiven Studien erstaunlich gut . Wir versuchen in einem anderen Projekt, diesen Mangel durch einen 3-D-Drucker auszugleichen, mit dem wir Tumorzellen plus Matrix plus Makrophagen plus Immunzellen „drucken“ können. Ob sich dadurch tatsächlich das Tumoransprechen besser vorhersagen lässt, wissen wir nicht. Man kann das sehr gut mit Modellzelllinien machen, aber mit patienteneigenen Zellen ist das schwierig, weil diese unterschiedlich gut außerhalb des Körpers überleben.
Wie lange dürfen Organoide vermehrt werden, damit klonale Heterogenität fortbesteht?
Um zu vermeiden, dass man durch Zellkultur bestimmte Klone selektioniert, ist man bestrebt, niedrige Passagen zu wählen. Für unsere Testung ist das kein Problem, weil wir etablieren und sofort testen. Wir wählen also die niedrigstmögliche Passage.
Ein überall gültiges SOP für Organoide unterstellt: Es ist egal, wann und in welchem Zustand biopsiert wird
Egal ist es nicht, weil der Zeitpunkt der Biopsie-Entnahme das natürlich erheblich bestimmt. Ob es gelingt, ein Organoid aus einer Tumorprobe zu etablieren, hängt u. a. davon ab, ob und wie viele Chemotherapiezyklen der Patient oder die Patientin bekommen hat. Je mehr Vorbehandlungen, umso schwieriger wird es, Organoide zu etablieren. Wir können auch Organoide aus Metastasen einfacher gewinnen als aus dem Primärtumor Es gibt einige Aspekte an der Technologie, die wir noch nicht vollständig verstehen.
Angesichts des komplexen Verfahrens – Ist es realistisch, dieses in die Klinik zu bringen?
Ist es praktikabel? Ich denke, ja. Es ist realistisch, dass man es schafft. Wichtig ist zu sehen, wie häufig man es schafft, zu 90, 100 oder zu 50 Prozent. Unsere Patientinnen und Patienten erhalten immer die bestmögliche Therapie, auch wenn es nicht gelingt, ein Organoid zu etablieren. Wenn genügend Daten vorliegen und man damit Modelle trainieren kann, werden wir vielleicht Prädiktoren definieren können, die in Zukunft eine Testung direkt am Tumormaterial ermöglichen, ohne den „Umweg“ über Organoide.