Neurodegenerative Erkrankungen
Blutbasierte Biomarker erlauben frühzeitige Risikoprognose für Alzheimer
Die meisten Demenzerkrankungen entwickeln sich schleichend und werden erst spät erkannt. Forschende der Universität Heidelberg und des Deutschen Krebsforschungszentrums identifizierten jetzt im Blut das saure Gliafaserprotein (GFAP) als vielversprechenden Biomarker, mit dessen Hilfe das erhöhte Risiko für die Entwicklung einer Alzheimer-Demenz bis zu 17 Jahre vor der Diagnose ermittelt werden kann.
Je länger wir leben, desto häufiger ist auch unser Gehirn von pathologischen Veränderungen betroffen. Bis zu einem gewissen Grad sind eingeschränkte Funktionen der Nervenzellen und sogar das Absterben von Neuronen normale Alterserscheinungen, die nur milde Symptome hervorrufen. Treten diese Ereignisse aber verstärkt auf, so können erhebliche Störungen der Motorik oder gravierende Gedächtnisverluste die Folge sein.
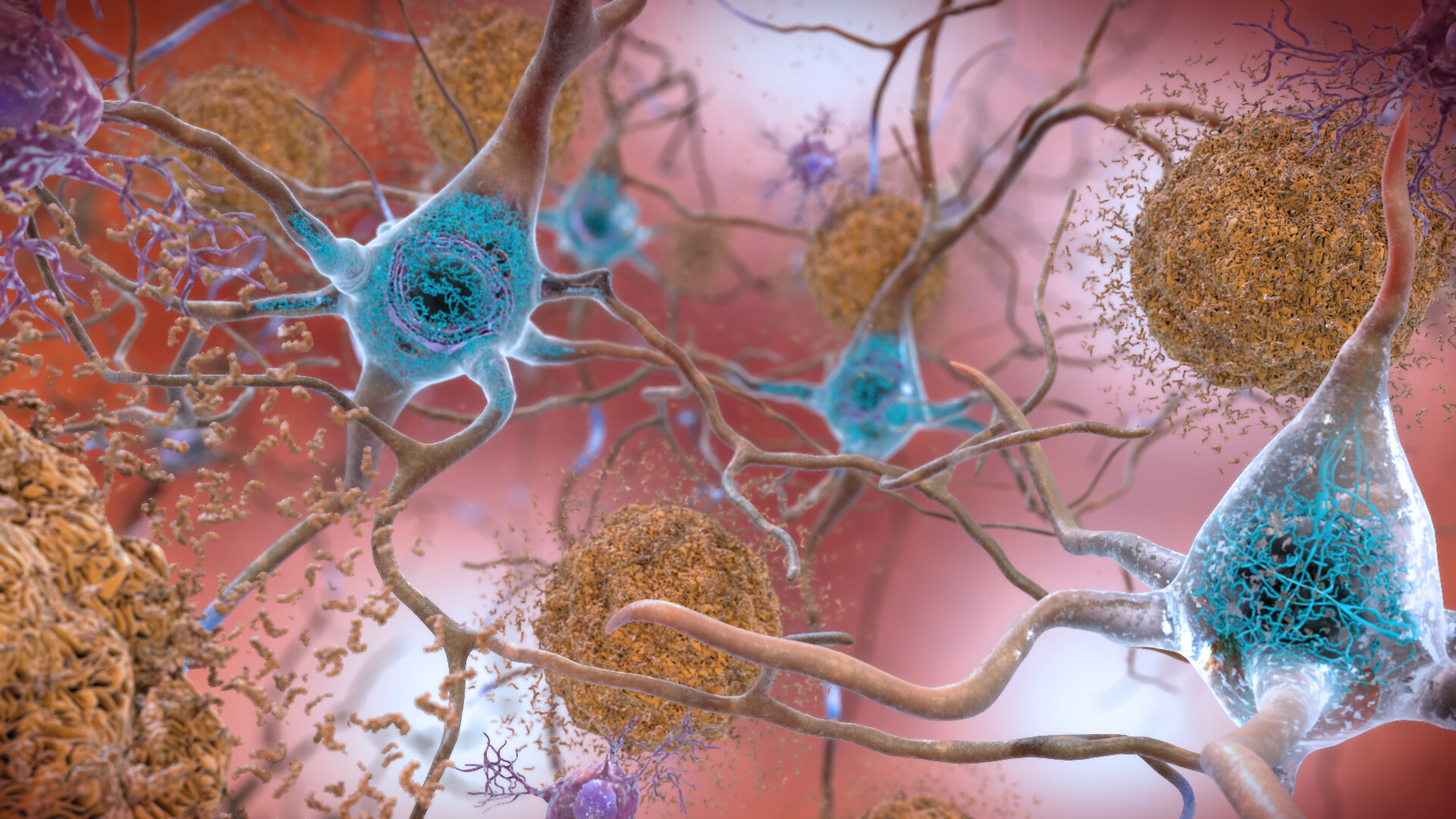 Im Gehirn von Personen mit Alzheimer-Erkrankung verklumpen Beta-Amyloid-Peptide und formen senile Plaques (braun) in den Zellzwischenräumen. Innerhalb der Zellen aggregiert abnormal phosphoryliertes Tau-Protein und bildet Fibrillen (blau). Quelle: flickr.com (2022) I National Institute on Aging, NIH I Public Domain Werk
Im Gehirn von Personen mit Alzheimer-Erkrankung verklumpen Beta-Amyloid-Peptide und formen senile Plaques (braun) in den Zellzwischenräumen. Innerhalb der Zellen aggregiert abnormal phosphoryliertes Tau-Protein und bildet Fibrillen (blau). Quelle: flickr.com (2022) I National Institute on Aging, NIH I Public Domain WerkDie Alzheimer-Krankheit (Alzheimer’s disease AD) ist mit einem Anteil von mehr als 60 Prozent die häufigste Form der Demenz.1) Bei ihr lagern sich Beta-Amyloid-(Aβ-)Peptide in Form von sogenannten senilen Plaques zwischen den Neuronen der grauen Hirnsubstanz ab. Die Proteinfragmente entstehen kontinuierlich beim Abbau des Amyloid-Precursor-Proteins, das vor allem in den Membranen von Nervenzellen vorkommt. Eine mit zunehmendem Alter veränderte Stoffwechsellage kann dazu führen, dass Aβ nicht mehr vollständig abgebaut wird und sich deshalb ansammelt. Als Folge verstärkt sich in den Nervenzellen die Phosphorylierung des Tau-Proteins, das für die Bildung der stützenden Mikrotubuli des Zytoskeletts wichtig ist. Im Zytoplasma kommt es daraufhin zur Verklumpung der pTau-Proteine und Entstehung von sogenannten Alzheimer-Fibrillen. Beide Eiweißablagerungen stören die Kommunikation innerhalb und zwischen den Nervenzellen irreversibel und führen letztendlich zum Absterben der Neuronen (Neurodegeneration).
Lange konnten die krankhaften Veränderungen im Gehirn erst nach dem Tod der Betroffenen nachgewiesen werden, und die Diagnose erfolgte ausschließlich anhand der Symptome. Heutzutage ist zusätzlich eine Bestimmung von Aβ und pTau aus der Gehirn-Rückenmarksflüssigkeit (Liquor) möglich oder auch die Visualisierung der Plaques und Fibrillen mittels Positronen-Emissions-Tomografie (PET). Beide Verfahren sind allerdings aufwendig und kostspielig und nicht für den breiten Einsatz geeignet. Da zudem immer deutlicher wird, dass die pathologischen Prozesse schon lange vor den ersten Symptomen einsetzen, ist für die frühe Beurteilung eine einfache, nichtinvasive Methode nötig.
„Unser Hauptinteresse ist es, einen verlässlichen Weg für die Risikoabschätzung einer Alzheimer-Erkrankung zu finden, der sich gut in den Kliniken umsetzen lässt“, berichtet Dr. Hannah Stocker vom Netzwerk Alternsforschung der Universität Heidelberg und Wissenschaftlerin in der von Prof. Dr. Hermann Brenner geleiteten Abteilung Klinische Epidemiologie und Alternsforschung des Deutschen Krebsforschungszentrum (DKFZ). Zu diesem Zweck nutzte sie Blutproben aus der ESTHER-Kohortenstudie (Epidemiologische Studie zu Chancen der Verhütung, Früherkennung und optimierten THerapie chronischer ERkrankungen in der älteren Bevölkerung), die seit dem Jahr 2000 unter Leitung von Brenner und dem Saarländischen Krebsregister durchgeführt wird.
Blutbasierte Biomarker zur frühen Erkennung pathologischer Prozesse
Die zusammen mit der Ruhr-Universität Bochum durchgeführten Untersuchungen konzentrierten sich auf bereits etablierte, biologisch relevante Moleküle, sogenannte Biomarker, die in Zusammenhang mit AD stehen. Aβ eignet sich in diesem Fall nicht, da es schwierig zu messen und in Blutproben zudem instabil ist. Die an Position 181 phosphorylierte Version des Tau-Proteins (pTau181) hingegen gilt aufgrund mehrerer unabhängiger Studien als vielversprechender Kandidat, um AD früh zu diagnostizieren und von anderen Demenzen zu unterscheiden.2) Da die Mengen im Blut mit dem Schweregrad der Erkrankung korrelieren und erhöhte Werte an pTau181 bereits vor Auftritt klinischer Symptome nachweisbar sind, könnte das Protein zur Verlaufskontrolle, bzw. Risikoabschätzung geeignet sein.
Ein weiteres, bisher hauptsächlich aus Liquor bestimmtes Markerprotein ist NFL (Neurofilament Leichtkette). Hierbei handelt es sich um ein in den Nervenzellfortsätzen (Axonen) lokalisiertes Strukturprotein, das bei Entzündung oder Beschädigung der Zellen freigesetzt wird. Es ist allerdings nicht spezifisch für AD, sondern zeigt alle Arten der Neurodegeneration an (beispielsweise auch Multiple Sklerose) und dient deshalb vor allem zur Einstufung des Schweregrades. Auch das saure Gliafaserprotein (Glial fibrillary acidic protein GFAP) kann als Indikator für Demenz-assoziierte Veränderungen herangezogen werden. Es ist Bestandteil der zytosolischen Filamente von Gliazellen (vor allem Astrozyten), die das Stützgewebe des Nervensystems bilden. Erhöhte Werte im Blut zeigen eine Aktivierung der Astrozyten an und wurden bisher als Nachweis für Hirntumore genutzt. Neuere Ergebnisse weisen darauf hin, dass die Spiegel auch aufgrund von Aβ-Ablagerungen ansteigen können.
GFAP ist bereits bis zu 17 Jahre vor Diagnose erhöht
 Dr. Hannah Stocker identifizierte zusammen mit anderen Forschenden GFAP als potenziellen Biomarker für die Alzheimer-Risikoprognose. © Universität Heidelberg
Dr. Hannah Stocker identifizierte zusammen mit anderen Forschenden GFAP als potenziellen Biomarker für die Alzheimer-Risikoprognose. © Universität HeidelbergFür die im März 2022 im Fachjournal Alzheimer’s & Dementia erschienene Publikation3) bestimmten Stocker und ihre Mitautorinnen und Mitautoren die Mengen von pTau181, NFL und GFAP in 768 Blutproben, die zu Beginn der ESTHER-Studie entnommen wurden. Sie stammen von Frauen und Männern, die zum damaligen Zeitpunkt zwischen 50 und 74 Jahre alt waren, und von denen ein Drittel im Verlauf der folgenden 17 Jahre eine Alzheimer-Diagnose erhielt. „Wir haben gesehen, dass die GFAP-Werte der später Erkrankten erhöht waren, auch wenn die Diagnose teilweise erst 14 bis 17 Jahre später gestellt wurde“, erläutert die Epidemiologin. „Erhöhte Spiegel von pTau181 und NFL hingegen kamen nur vor, wenn AD bereits innerhalb von neun Jahren auftrat. So einen frühen Anstieg und diesen deutlichen Unterschied zwischen den Markern hatten wir nicht erwartet.“ Die Ergebnisse offenbaren das große Potenzial des bisher weniger intensiv erforschten Biomarkers GFAP für die Risikoabschätzung.
„Es stehen allerdings noch einige Fragen im Raum“, führt Stocker aus, die seit Oktober 2022 am Deutschen Zentrum für Neurodegenerative Erkrankungen (DZNE) in Bonn tätig ist. „Bisher ist noch nicht genau geklärt, ob GFAP spezifisch für die Alzheimer-Krankheit ist oder eher allgemein Demenzerkrankungen anzeigt.“ Aus diesem Grund möchte sie in zukünftigen Projekten die Blutproben der Probandinnen und Probanden untersuchen, bei denen andere Demenzen aufgetreten sind. Des Weiteren ist die Analyse von Proben geplant, die zu späteren Zeitpunkten abgenommen wurden, um Aufschluss darüber zu bekommen, wie sich die Werte der Biomarker im zeitlichen Verlauf ändern. Stocker hebt hervor: „Die ESTHER-Kohortenstudie ist einzigartig, sowohl was ihren zeitlichen Rahmen von im Moment 20 Jahren als auch die Teilnehmerzahl von ursprünglich fast 10.000 Probanden betrifft.“ Langfristiges Ziel ist es, mithilfe der Biomarker Faktoren zu identifizieren, die die Zeit bis zum Ausbruch der Demenz beeinflussen können. Denn einige Personen bleiben trotz der Proteinablagerungen im Gehirn über Jahrzehnte symptomfrei.
Auch wenn es zum aktuellen Zeitpunkt keine Medikamente gibt, um neurodegenerative Erkrankungen zu heilen, so bietet die frühe Erkennung pathologischer Veränderungen die Chance, Symptome abzumildern bzw. ihr Auftreten hinauszuzögern. Für ein umfassendes Screeningverfahren ist es wichtig, verschiedene leicht zugängliche Biomarker zu identifizieren, sodass durch deren Kombination eine möglichst präzise Aussage über das Krankheitsrisiko getroffen werden kann. Die aktuellen Daten zeigen, dass GFAP hierfür ein vielversprechender Kandidat ist.